题目内容
欲配制100mL 0.2mol/L的NaOH溶液,回答下列问题:(1)根据计算,所需的NaOH的质量为 ,NaOH固体应放在 中称量.
(2)以下是实验操作步骤,请排出正确的操作顺序:
①称取所需质量的NaOH
②将溶液转移到容量瓶内
③用蒸馏水洗涤烧杯2~3次,将洗涤液全部移入容量瓶中,摇匀
④改用胶头滴管,小心滴入蒸馏水至刻度
⑤仔细地把蒸馏水注入容量瓶中,直到液面接近刻度线1cm~2cm处
⑥塞上瓶塞.反复摇匀
⑦将称取的NaOH置于烧杯内,加适量蒸馏水,搅拌溶解后冷却正确的操作顺序是:
(3)下列操作会使所配溶液浓度偏低的是 (填选项代号)
A.NaOH放在纸上称量,且出现潮解现象
B.配制前容量瓶内已有少量蒸馏水
C.定容时仰视
D.NaOH溶液未经冷却就转移到容量瓶中去
E.转移溶液时部分溶液溅出容量瓶外.
【答案】分析:(1)根据m=nM=cvM计算溶质的质量;根据NaOH固体的称量方法;
(2)根据实验操作的步骤;
(3)根据c=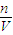 分析操作对溶质的物质的量或对溶液的体积的影响判断.
分析操作对溶质的物质的量或对溶液的体积的影响判断.
解答:解:(1)NaOH的质量m=nM=cvM=0.2mol/L×0.10L×40g/mol=8.0g,NaOH易潮解,需放在烧杯中称量,
故答案为:8.0g;小烧杯;
(2)配制时步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,故答案为:①⑦②③⑤④⑥;
(3)A.NaOH放在纸上称量,且出现潮解现象,溶质的质量减少,浓度偏小,故A正确;
B.配制前容量瓶内已有少量蒸馏水,无影响,浓度不变,故B错误;
C.定容时仰视,溶液体积偏大,浓度偏小,故C正确;
D.NaOH溶液未经冷却就转移到容量瓶中去,溶液冷却下来,溶液体积偏小,浓度偏大,故D错误;
E.转移溶液时部分溶液溅出容量瓶外,溶质的质量减少,浓度偏小,故E正确;
故答案为:ACE.
点评:本题考查了一定物质的量浓度溶液的配制以及误差分析,难度不大,注意根据c=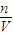 分析不当操作对n或V的影响.
分析不当操作对n或V的影响.
(2)根据实验操作的步骤;
(3)根据c=
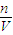 分析操作对溶质的物质的量或对溶液的体积的影响判断.
分析操作对溶质的物质的量或对溶液的体积的影响判断.解答:解:(1)NaOH的质量m=nM=cvM=0.2mol/L×0.10L×40g/mol=8.0g,NaOH易潮解,需放在烧杯中称量,
故答案为:8.0g;小烧杯;
(2)配制时步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,故答案为:①⑦②③⑤④⑥;
(3)A.NaOH放在纸上称量,且出现潮解现象,溶质的质量减少,浓度偏小,故A正确;
B.配制前容量瓶内已有少量蒸馏水,无影响,浓度不变,故B错误;
C.定容时仰视,溶液体积偏大,浓度偏小,故C正确;
D.NaOH溶液未经冷却就转移到容量瓶中去,溶液冷却下来,溶液体积偏小,浓度偏大,故D错误;
E.转移溶液时部分溶液溅出容量瓶外,溶质的质量减少,浓度偏小,故E正确;
故答案为:ACE.
点评:本题考查了一定物质的量浓度溶液的配制以及误差分析,难度不大,注意根据c=
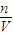 分析不当操作对n或V的影响.
分析不当操作对n或V的影响. 
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
欲配制100ml 0.10mol/L的NaCl溶液,一定需要使用的仪器是( )
| A、铁架台 | B、酒精灯 | C、分液漏斗 | D、100ml容量瓶 |
欲配制100ml 0.10mol/L的KCl溶液,不需要使用的仪器有( )
| A、玻璃棒 | B、烧杯 | C、分液漏斗 | D、100ml容量瓶 |