题目内容
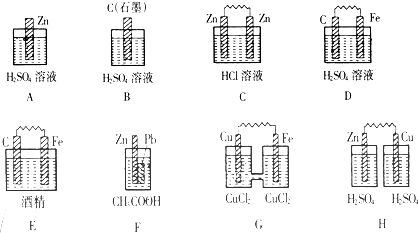
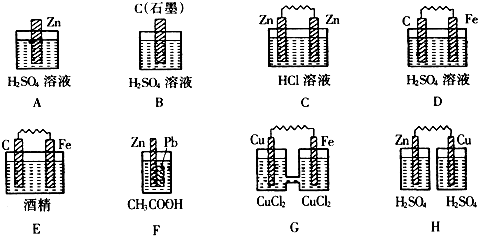
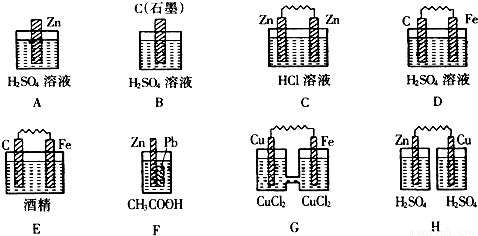
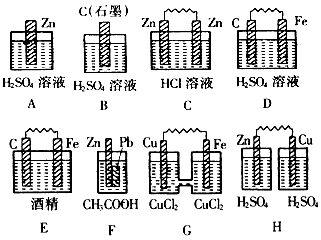
(1)在下图的装置中,属于原电池的是

(2)以锌、石墨棒为两极,硫酸铜溶液为电解液组成的原电池的正极反应式是
D、F、G
D、F、G

(2)以锌、石墨棒为两极,硫酸铜溶液为电解液组成的原电池的正极反应式是
Cu2++2e-=Cu
Cu2++2e-=Cu
,负极反应式是Zn-2e-=Zn2+.
Zn-2e-=Zn2+.
.分析:(1)原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,根据原电池的构成条件判断;
(2)原电池中较不活泼的金属或导电的非金属作正极,正极上得电子;较活泼的金属作负极,负极失电子生成离子进入溶液.
(2)原电池中较不活泼的金属或导电的非金属作正极,正极上得电子;较活泼的金属作负极,负极失电子生成离子进入溶液.
解答:解:(1)A、B中没有两个活泼性不同的电极,故A、B错误;
C、两个电极材料相同,故C错误;
E、酒精不是电解质,故E错误;
H、没有构成闭合回路,故H错误;
D、F、G符合原电池的构成条件,故D、F、G正确;
故答案为:D、F、G;
(2)该原电池中石墨作正极,正极上铜离子得电子生成铜单质,电极反应式为Cu2++2e-=Cu;
锌作负极,锌失电子生成锌离子进入溶液,电极反应式为 Zn-2e-=Zn2+.
故答案为:Cu2++2e-=Cu;Zn-2e-=Zn2+.
C、两个电极材料相同,故C错误;
E、酒精不是电解质,故E错误;
H、没有构成闭合回路,故H错误;
D、F、G符合原电池的构成条件,故D、F、G正确;
故答案为:D、F、G;
(2)该原电池中石墨作正极,正极上铜离子得电子生成铜单质,电极反应式为Cu2++2e-=Cu;
锌作负极,锌失电子生成锌离子进入溶液,电极反应式为 Zn-2e-=Zn2+.
故答案为:Cu2++2e-=Cu;Zn-2e-=Zn2+.
点评:本题考查了原电池的判断及电极反应式的书写,难度不大,写电极反应式要注意结合电解质溶液书写,如果电解质溶液不同,虽然原料相同,电极反应式也不同,如氢氧燃料电池,当电解质为酸或碱,电极反应式就不同.

练习册系列答案
相关题目