题目内容
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”。请分别用下图中示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6 mol·L-1盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去)。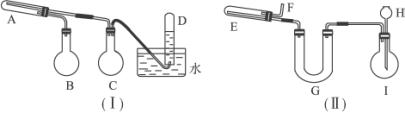
填写下列空白:
(1)实验进行时试管A中应加入的试剂是_____________,烧瓶B的作用是_______________,烧瓶C的作用是________________________,在试管D中收集得到的是________________。
(2)实验时,U形管G中应加入的试剂是_____________,长颈漏斗H中应加入_____________。
(3)两套装置中,在实验时需要加热的仪器是(填该仪器对应的字母) ___________________。
(4)烧瓶I中发生的反应有时要加入少量硫酸铜溶液,其目的是_________________________。
(5)试管E中发生反应的化学方程式是_____________________________________________。
(6)为了安全,在E管中的反应发生前,在F出口处必须________________;E管中的反应开始后,在F出口处应________________________________。
(1)普通铁粉(或铁粉) 作为水蒸气发生器(或用来产生水蒸气) 防止水倒吸(或用作安全瓶) 氢气
(2)固体NaOH(或碱石灰、CaO等碱性固体干燥剂) 6 mol·L-1 HCl
(3)ABE
(4)加快氢气产生的速率
(5)Fe3O4+4H2![]() 3Fe+4H2O
3Fe+4H2O
(6)检验氢气的纯度 点燃氢气
解析:首先明确本题涉及的3个反应:①普通铁粉的高温氧化:3Fe+4H2O(g) ![]() Fe3O4+4H2;②四氧化三铁的热还原:Fe3O4+4H2
Fe3O4+4H2;②四氧化三铁的热还原:Fe3O4+4H2![]() 3Fe+4H2O;③用6 mol·L-1HCl与较活泼金属(例如锌)制备上述反应所需的还原剂氢气:Zn+2HCl====ZnCl2+H2↑。题目给出了两个装置图,左图内有生成物排水取气的装置,右图内则有发生氢气的装置。由此可判断出,前者为制取四氧化三铁的装置,后者为制取“引火铁”的装置。
3Fe+4H2O;③用6 mol·L-1HCl与较活泼金属(例如锌)制备上述反应所需的还原剂氢气:Zn+2HCl====ZnCl2+H2↑。题目给出了两个装置图,左图内有生成物排水取气的装置,右图内则有发生氢气的装置。由此可判断出,前者为制取四氧化三铁的装置,后者为制取“引火铁”的装置。
试管A里装入的试剂是普通铁粉,烧瓶B的作用是作为水蒸气发生器,烧瓶C的作用是作为安全瓶防止水槽内的冷水倒吸,收集在试管D内的气体当然是氢气。
在右图中,由于盐酸较浓(6 mol·L-1),与活泼金属反应所产生的氢气中或多或少地会带有部分盐酸酸雾,如不除去盐酸酸雾,则其会跟四氧化三铁发生反应,所以U形管内应该用固体氢氧化钠或氧化钙、碱石灰等碱性干燥剂,以除去酸雾。至于6 mol·L-1盐酸,当然应从长颈漏斗加入作为气体发生器的烧瓶内。
烧瓶B是水蒸气发生器,为将其中的水变为蒸气,当然需要加热。普通铁粉被水蒸气氧化是在高温进行的反应,四氧化三铁被氢气还原需在加热条件下进行,因此A、B、E都需加热。
在烧瓶I中加入硫酸铜溶液,目的在于使跟盐酸反应的金属Zn表面因与硫酸铜置换而部分覆盖金属铜,形成铜锌原电池,加快了氢气产生的进程。
为保证安全,进入试管E内的氢气必须是纯氢气,因而需验纯。自导管F逸入空气中的氢气应烧掉或导出室外,以避免与室内的空气发生爆炸。

 在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉.现用下图中甲、乙两套仪器装置制取上述铁的氧化物和细铁粉.制取上述铁的氧化物和细铁粉时必须使用普通铁粉和6mol?L-1盐酸,其他试剂任选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热装置等以及仪器中所装的试剂在图中均已略去).
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉.现用下图中甲、乙两套仪器装置制取上述铁的氧化物和细铁粉.制取上述铁的氧化物和细铁粉时必须使用普通铁粉和6mol?L-1盐酸,其他试剂任选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热装置等以及仪器中所装的试剂在图中均已略去).


