题目内容
下列第三周期元素的离子中,半径最小的是( )
| A、Na+ |
| B、Al3+ |
| C、S2- |
| D、Cl- |
考点:微粒半径大小的比较
专题:元素周期律与元素周期表专题
分析:离子电子层结构相同,核电荷数越大离子半径越大,离子电子层越多,离子半径越大.
解答:
解:Na+、Al3+电子层结构相同,S2-、Cl-电子层结构相同,核电荷数越大离子半径越小,故离子半径Na+>Al3+,S2->Cl-,S2-、Cl-比Na+、Al3+多一个电子层,离子电子层越多,离子半径越大,故离子半径:S2->Cl->Na+>Al3+,离子半径最小的是Al3+,
故选B.
故选B.
点评:本题考查离子半径比较,难度不大,侧重对基础知识的巩固,掌握比较规律即可解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法正确的是( )
| A、分子量相同的两种不同分子一定互为同分异构体 |
| B、各元素质量分数均相同的两种不同分子一定互为同分异构体 |
| C、同分异构体的物理性质一定相同 |
| D、互为同系物的两种分子不可能互为同分异构体 |
对如图所示的实验装置的判断中错误的是( )
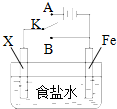

| A、若X为碳棒,开关K置于A处可减缓铁的腐蚀 |
| B、若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀 |
| C、若X为锌棒,开关K置于B处时,为牺牲阳极的阴极保护法 |
| D、若X为碳棒,开关K置于B处时,碳棒上发生的反应为2H++2e-═H2↑ |
下列各组物质既不是同系物又不是同分异构体的是( )
| A、果糖和蔗糖 |
| B、甲酸甲酯和乙酸 |
| C、对甲基苯酚和苯甲醇 |
| D、乙二醇和丙二醇 |
下列各原子中,半径最大的是( )
| A、Cl | B、S | C、P | D、Si |
美国天文学害在亚利桑那州一天文观察台探测到了银河系中心2.6万光年处一巨大气云中的特殊电磁波,这种电磁波表明那里可能有乙醇醛糖分子存在.下列有关乙醇醛糖(HOCH2CHO)的有关说法不正确的是( )
| A、乙醇醛糖是一种有机物,易溶于水 |
| B、1mol 乙醇醛糖与足量的银氨溶液作用,可析出2mol Ag |
| C、乙醇醛糖与甲酸甲酯互为同分异构体 |
| D、乙醇醛糖能发生取代反应、消去反应、氧化反应以及还原反应 |
下列说法正确的是( )
| A、实验室从海带提取单质碘的方法是:取样、灼烧、溶解、过滤、萃取 |
| B、用乙醇和浓制备乙烯时,可用水浴加热控制反应的温度 |
| C、在室温下,向氯化银的沉淀溶解平衡的体系中加入蒸馏水,氯化银的Ksp保持不变 |
| D、将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性 |
要证明氯乙烷中氯元素的存在可进行如下操作,其中顺序正确的是( )
①加入AgNO3溶液 ②加入NaOH溶液 ③加热 ④加入蒸馏水 ⑤加入HNO3酸化.
①加入AgNO3溶液 ②加入NaOH溶液 ③加热 ④加入蒸馏水 ⑤加入HNO3酸化.
| A、②③⑤① | B、④③⑤① |
| C、④①⑤ | D、②③①⑤ |