题目内容
区分胶体和溶液的常用方法是
A. 观察颜色 B. 一束光照射 C. 静置 D. 过滤
 阅读快车系列答案
阅读快车系列答案2CH3CH2CH2CH2OH (CH3CH2CH2CH2)2O + H2O。反应物和产物的相关数据如下
(CH3CH2CH2CH2)2O + H2O。反应物和产物的相关数据如下
| 相对分子质量 | 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 |
正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
合成反应:
①将6 mL浓硫酸和37 g正丁醇,按一定顺序添加到A中,并加几粒沸石。
②加热A中反应液,迅速升温至135℃,维持反应一段时间。
分离提纯:
③待A中液体冷却后将其缓慢倒入盛有70 mL水的分液漏斗中,振荡后静置,分液得粗产物。
④粗产物依次用40 mL水、20 mL NaOH溶液和40 mL水洗涤,分液后加入约3 g无水氯化钙颗粒,静置一段时间后弃去氯化钙。
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11 g。
请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为 。
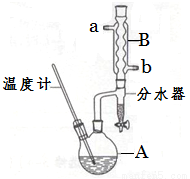
(2)加热A前,需先从 (填“a”或“b”)口向B中通入水。
(3)步骤③的目的是初步洗去 ,振荡后静置,粗产物应从分液漏斗的 (填“上”或“下”)口分离出。
(4)步骤④中最后一次水洗的目的为 。
(5)步骤⑤中,加热蒸馏时应收集 (填选项字母)左右的馏分。
a.100℃ b. 117℃ c. 135℃ d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A。分水器中上层液体的主要成分为 ,下层液体的主要成分为 。
(7)本实验中,正丁醚的产率为 。(保留两位有效数字)
氯化铁可用作金属蚀刻、有机合成的催化剂,研究其制备及性质是一个重要的课题。
(1)氯化铁晶体的制备:

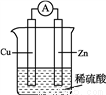
①实验过程中装置乙发生反应的离子方程式有________,仪器丙的作用为_________。
②为顺利达成实验目的,上述装置中弹簧夹打开和关闭的顺序为_______________。
③反应结束后,将乙中溶液边加入_____________,边进行加热浓缩、______、过滤、洗涤、干燥即得到产品。
(2)氯化铁的性质探究:
某兴趣小组将饱和FeC13溶液进行加热蒸发、蒸干灼烧,在试管底部得到固体。为进一步探究该固体的成分设计了如下实验。(查阅文献知:①FeC13溶液浓度越大,水解程度越小 ②氯化铁的熔点为306℃、沸点为315℃ ,易升华,气态FeCl3会分解成FeCl2和Cl2③ FeC12熔点670℃)

操作步骤 | 实验现象 | 解释原因 |
打开K , 充入氮气 | D中有气泡产生 | ①充入N2的原因________ |
关闭K, 加热至600℃,充分灼烧固体 | B中出现棕黄色固体 | ②产生现象的原因__________ |
实验结束,振荡C静置 | ③___________ | ④________________(用相关的方程式说明) |
⑤结合以上实验和文献资料,该固体可以确定的成分有______________________。 | ||


 B. NaCl的电子式:Na∶Cl
B. NaCl的电子式:Na∶Cl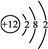 D. 硫酸铁的电离方程式:Fe2(SO4)3===2Fe2++3SO
D. 硫酸铁的电离方程式:Fe2(SO4)3===2Fe2++3SO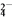
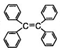 )中所有碳原子一定处于同一平面
)中所有碳原子一定处于同一平面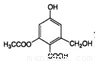 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3mol、4mol、1mol
分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3mol、4mol、1mol 2C(g) ΔH<0,若起始温度相同,分别向三个容器中通入3molA和1molB,则达到平衡时各容器中C物质的体积分数由大到小的顺序为 ( )
2C(g) ΔH<0,若起始温度相同,分别向三个容器中通入3molA和1molB,则达到平衡时各容器中C物质的体积分数由大到小的顺序为 ( )