题目内容
【题目】下列实验装置图,其中关于用途的描述,不正确的是( )
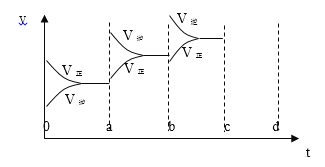
A. 装置:收集二氧化碳,从a口进气b口排气
装置:收集二氧化碳,从a口进气b口排气
B. 装置:用于石油的分馏
装置:用于石油的分馏
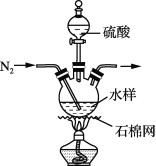
C. 装置:用于分离Cl2与KI溶液反应生成的碘
装置:用于分离Cl2与KI溶液反应生成的碘
D. 装置:可用来制取氨气
装置:可用来制取氨气
【答案】C
【解析】
A. 二氧化碳密度比空气大;
B. 冷凝水下进上出;
C. 分离出Cl2与KI溶液反应生成的碘,碘单质易溶于有机物,在水中溶解度不大;
D. 氧化钙与水反应放热,结合氨水中存在的平衡分析。
A. 二氧化碳密度比空气大,可用向上排空气法收集,长进短出,A正确;
B. 为了充分冷凝,采用逆流原理,冷凝水下进上出,温度计水银球位于蒸馏烧瓶支管口处,测定蒸气温度,操作合理,B正确;
C. 因氧化性Cl2>I2,所以Cl2会把KI中的I-置换出来:Cl2+2KI=2KCl+I2,生成的碘能溶于水,用过滤的方法无法分离氯化钾和碘水,利用I2易溶于有机物,在水中溶解度不大,应该向其中加入CCl4或苯作萃取剂,然后再进行分液的方法,C错误;
D. 氧化钙与水反应放热,可促进一水合氨分解,产生氨气;二者反应产生的Ca(OH)2电离产生的OH-也促使平衡向产生氨气的方向移动,可用来制取氨气,D正确;
故答案选C。

练习册系列答案
相关题目