题目内容
[实验一]测定硫元素的含量.
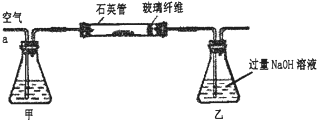
Ⅰ、将m1g该黄铁矿样品放入如右图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全.石英管中发生反应的化学方程式为:4FeS2+11O2═2Fe2O3+8SO2
Ⅱ、反应结束后,将乙瓶中的溶液进行如下处理:
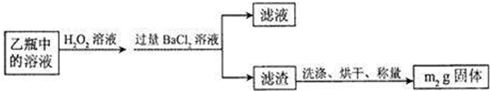
[实验二]测定铁元素的含量.
III、测定铁元素含量的实验步骤如图所示.
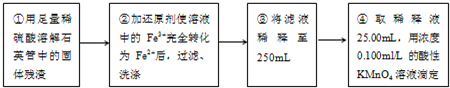
问题讨论:
(1)I中,甲瓶内所盛试剂是
(2)II中,乙瓶加入H2O2溶液时反应的离子方程式为
(3)该黄铁矿中硫元素的质量分数为
| 32m2 |
| 233m1 |
| 32m2 |
| 233m1 |
(4)III的步骤③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有
(5)III的步骤④中,表示滴定已达终点的现象是
(6)Ⅲ的步骤④进行了三次平行实验,测得消耗KMnO4溶液体积分别为24.98mL、24.80mL、25.02mL(KMnO4被还原为Mn2+).根据上述数据,可计算出该黄铁矿样品铁元素的质量分数为
| 7 |
| m1 |
| 7 |
| m1 |
(2)过氧化氢具有强氧化性,将亚硫酸根离子氧化为硫酸根,同时生成水;
(3)最终得到的沉淀为硫酸钡,根据硫原子守恒计算硫铁矿中硫的质量,从而计算其质量分数;
(4)配制250ml一定物质的量浓度的溶液需要烧杯、玻璃棒、胶头滴管、量筒、250ml容量瓶等仪器;
(5)最后一滴高锰酸钾溶液滴入时,溶液颜色突变为紫色,且在30s内不变色,说明滴定到达终点;
(6)令硫铁矿中铁元素的质量分数为a,根据关系式MnO4-~5Fe2+~5Fe计算硫铁矿中铁元素的质量分数.
故答案为:NaOH;SO2+2OH-=SO32-+H2O、2SO32-+O2=2SO42-;
(2)过氧化氢具有强氧化性,将亚硫酸根离子氧化为硫酸根,同时生成水,反应离子方程式为:SO32-+H2O2═SO42-+H2O,
故答案为:SO32-+H2O2═SO42-+H2O;
(3)根据硫元素守恒,m1gFeS2中的硫元素最终全部生成BaSO4,则有n(BaSO4)=
| m2 |
| 233 |
| m2 |
| 233 |
| ||
| m1 |
| 32m2 |
| 233m1 |
故答案为:
| 32m2 |
| 233m1 |
(4)Ⅲ的步骤③中,一定物质的量浓度溶液的配制中,除了烧杯、玻璃棒、胶头滴管外,还需要250mL容量瓶,
故答案为:250mL容量瓶;
(5)最后一滴高锰酸钾溶液滴入时,溶液颜色突变为紫色,且在30s内不变色,说明滴定到达终点,
故答案为:最后一滴高锰酸钾溶液滴入时,溶液颜色突变为紫色,且在30s内不变色;
(6)令硫铁矿中铁元素的质量分数为a,则:
MnO4-~5Fe2+~5Fe
1mol 5×56g
0.1mol/L×25×10-3L×10 m1a g
所以1mol:0.1mol/L×25×10-3L×10=5×56g:m1a g
解得a=
| 7 |
| m1 |
故答案为:
| 7 |
| m1 |

| |||||||||||||||||||
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。目前我国已经在技术上取得突破——从硫酸渣中分离出各种成分并加以利用。其流程和相关数据如下:

查资料得知:
|
物质名称 |
溶度积(Ksp) |
pH值 |
|
|
开始沉淀 |
完全沉淀 |
||
|
Mg(OH)2 |
5.6×10-12 |
9.3 |
10.8 |
|
Fe(OH)3 |
2.8×10-16 |
2.7 |
3.7 |
|
Al(OH)3 |
1.3×10-33 |
3.7 |
4.7 |
请回答下列问题:
(1)写出固体A的化学式为 。
(2)若要测定溶液的pH是否达到3.7,下列实验用品中可选用的是 。
A.石蕊试液 B.广泛pH试纸 C.精密pH试纸 D.pH计
(3)完成下列离子反应方程式
①溶液D生成固体E ; ②溶液F生成固体G 。
(4)要将固体C、固体E和固体G都转化为相应的稳定氧化物,需进行的实验操作为 。
(5)若不考虑溶液体积的变化,请计算溶液H中c(Mg2+)= 。