题目内容
14.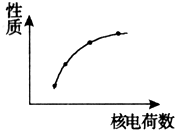 如图表示第IA族的金属元素的某些性质随核电荷数的变化关系.下列各性质中不符合图示关系的是( )
如图表示第IA族的金属元素的某些性质随核电荷数的变化关系.下列各性质中不符合图示关系的是( )| A. | 金属性 | B. | 阳离子的氧化性 | ||
| C. | 单质与水反应的剧烈程度 | D. | 最高价氧化物对应的水化物的碱性 |
分析 依据同主族元素从上到下,金属性依次增强,单质与水反应越剧烈,阳离子氧化性越弱,原子半径越大,最高价氧化物对应的水化物的碱性增强,以此来解答.
解答 解:ⅠA金属(又称为碱金属)位于同主族,同主族元素从上到下,金属性依次增强,单质与水反应越剧烈,阳离子氧化性越弱,原子半径越大,最高价氧化物对应的水化物的碱性增强,
故选:B.
点评 本题考查了碱土金属的性质,熟悉元素周期律,明确同主族元素性质的递变规律是解题关键,题目难度不大.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
4.对于下列甲、乙、丙三物质的说法,不正确的是( )

| A. | 等物质的量的甲、乙、丙分别与足量钠反应,乙放出气体最多 | |
| B. | 甲、乙、丙均能与Fe3+显色 | |
| C. | 甲和丙互为同分异构体 | |
| D. | 甲、乙、丙苯环上的一溴代物均为4种 |
5.实验室里做钠跟水反应的实验时,用到的仪器和药品是( )
①试管夹 ②镊子 ③小刀 ④滤纸 ⑤烧杯 ⑥石棉网⑦玻璃片 ⑧药匙.
①试管夹 ②镊子 ③小刀 ④滤纸 ⑤烧杯 ⑥石棉网⑦玻璃片 ⑧药匙.
| A. | ①②③④ | B. | ②③④⑤⑦ | C. | ①③④⑥⑧ | D. | ②⑤⑥⑦⑧ |
2.某主族元素的原子最外层只有一个电子,核外共有五个电子层,下列描述不正确的是( )
| A. | 该元素单质在常温下与水反应不如钠剧烈 | |
| B. | 该元素单质在常温下能与氧气反应 | |
| C. | 该元素最高化合价为+1 | |
| D. | 该元素氢氧化物的水溶液为强碱 |
9.用NA表示阿伏加德罗常数的数值,则下列说法中正确的是( )
| A. | 常温常压下,22.4L氧气含分子数为NA个O2 | |
| B. | 1molNa2O2化合物中有2mol阴离子和2mol阳离子 | |
| C. | 2.3g金属钠变为钠离子失去电子数为0.1NA | |
| D. | .常温下,1 L 0.5 mol•L-1 NH4Cl溶液中含有3.01×1023个NH4+ |
6.下列叙述正确的是( )
| A. | 25℃时,溶液中由水电离的c(H+)=1.0×10-4mol/L,则该溶液有可能是稀盐酸 | |
| B. | NH4Cl溶液加水稀释后,恢复至原温度,pH和Kw均增大 | |
| C. | pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等 | |
| D. | 在Na2S溶液中加入AgCl固体,白色AgCl转变为黑色Ag2S,则溶液中c(S2-)下降 |
3.下列物质中,能产生丁达尔现象的是( )
| A. | 氯酸钾溶液 | B. | 雾 | C. | 石灰乳 | D. | 油水混合物 |