��Ŀ����
����Ŀ�������������г���������,��ش���������:
(1)д��������ˮ��Һ�е���ķ���ʽ:_________��
(2)���������������������������е�_____��
(3)���� 10.6 g ��������ʵ���Ϊ__________mol�����˹�������ˮ��� 200 mL ��Һ,�����ʵ��� �ʵ���Ũ��Ϊ_________ mol��L-1��ȡ�� 10 mL ����Һ��ˮϡ���� 100 mL�������ʵ����ʵ���Ũ�� Ϊ___ mol��L-1��ϡ�ͺ���Һ�� Na+�����ʵ���Ϊ________ mol��
(4)��д������ CO2 �� NaOH ��Һ��Ӧ�����ӷ���ʽ: _____________
��д������ CO2 �� NaOH ��Һ��Ӧ�����ӷ���ʽ: _________________
���𰸡�Na2CO3=2Na++ CO32- �� 0.1 0.5 0.05 0.01 CO2+2OH-=CO32-+H2O CO2+OH-=HCO3-
��������
(1) ������̼���ƣ�ˮ��Һ�е������������Ӻ�̼������ӣ�
(2) ���̼���ƣ����ɽ��������Ӻ����������ɵĻ���������Σ�
(3) 10.6g��������ʵ���Ϊ![]() =0.1mol�����˹�������ˮ���200mL��Һ�������ʵ����ʵ���Ũ��Ϊ
=0.1mol�����˹�������ˮ���200mL��Һ�������ʵ����ʵ���Ũ��Ϊ![]() =0.5mol/L����ϡ�Ͷ��ɿɵã�0.5 mol/L ��10ml=c2��100ml��ϡ�ͺ����ʵ����ʵ���Ũ��c2=0.05mol/L��ϡ�ͺ���Һ�е�Na+���ʵ���Ϊ0.05 mol/L��0.1L��2=0.01mol��
=0.5mol/L����ϡ�Ͷ��ɿɵã�0.5 mol/L ��10ml=c2��100ml��ϡ�ͺ����ʵ����ʵ���Ũ��c2=0.05mol/L��ϡ�ͺ���Һ�е�Na+���ʵ���Ϊ0.05 mol/L��0.1L��2=0.01mol��
(4)��д������ CO2 �� NaOH ��Һ��Ӧ����̼���ƺ�ˮ��
��д������ CO2 �� NaOH ��Һ��Ӧ����̼�����ơ�
(1) ������̼���ƣ�ˮ��Һ�е������������Ӻ�̼������ӣ�����ķ���ʽ: Na2CO3=2Na+ + CO32-��
�ʴ�Ϊ��Na2CO3=2Na++CO32-��
(2) ���̼���ƣ����ɽ��������Ӻ����������ɵĻ���������Σ�
�ʴ�Ϊ���Σ�
(3) 10.6g��������ʵ���Ϊ![]() =0.1mol�����˹�������ˮ���200mL��Һ�������ʵ����ʵ���Ũ��Ϊ
=0.1mol�����˹�������ˮ���200mL��Һ�������ʵ����ʵ���Ũ��Ϊ![]() =0.5mol/L����ϡ�Ͷ��ɿɵã�0.5 mol/L ��10mL=c2��100mL��ϡ�ͺ����ʵ����ʵ���Ũ��c2=0.05mol/L��ϡ�ͺ���Һ�е�Na+���ʵ���Ϊ0.05 mol/L��0.1L��2=0.01mol��
=0.5mol/L����ϡ�Ͷ��ɿɵã�0.5 mol/L ��10mL=c2��100mL��ϡ�ͺ����ʵ����ʵ���Ũ��c2=0.05mol/L��ϡ�ͺ���Һ�е�Na+���ʵ���Ϊ0.05 mol/L��0.1L��2=0.01mol��
�ʴ�Ϊ��0.1��0.5��0.05��0.01��
(4)��д������ CO2 �� NaOH ��Һ��Ӧ����̼���ƺ�ˮ�����ӷ���ʽ: CO2+2OH-=CO32-+H2O��
�ʴ�Ϊ��CO2+2OH-=CO32-+H2O��
��д������ CO2 �� NaOH ��Һ��Ӧ����̼�����ƣ����ӷ���ʽ: CO2+OH-=HCO3-��
�ʴ�Ϊ��CO2+OH-=HCO3-��

 �������Ͽ��㱾ϵ�д�
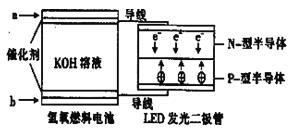
�������Ͽ��㱾ϵ�д�����Ŀ����a��b��c��d�ĸ������缫��GΪ�����ơ��йصķ�Ӧװ�ü����ַ�Ӧ�������£�
ʵ��װ�� |
|
|
|
|
����ʵ������ | a��������С��b���������� | ��Һ�е�SO42-��b���ƶ� | d���ܽ�c����������� | ���Ӵ�d������a�� |
�ɴ˿��ж������ֽ����Ļ��˳����
A. d>a>b>cB. a>b>c>dC. b>c>d>aD. a>b>d>c