题目内容
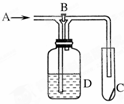 如图所示,从A处通入干燥的氯气.若打开活塞B,C中红色布条颜色无变化;若关闭活塞B,C中红色布条颜色褪去.则D瓶中盛有的溶液是( )
如图所示,从A处通入干燥的氯气.若打开活塞B,C中红色布条颜色无变化;若关闭活塞B,C中红色布条颜色褪去.则D瓶中盛有的溶液是( )| A、浓硫酸 | B、饱和食盐水 | C、氢氧化钠溶液 | D、浓NaI溶液 |
分析:干燥氯气不能使有色布条褪色,氯气能使有色布条褪色的原因是:氯气和水反应生成具有漂白性的HClO,先打开活塞B,在A处通入干燥氯气,干燥氯气不能使有色布条褪色,所以C中红色布条颜色无变化,再关闭活塞B,继续在A处通入干燥氯气,气体经过D装置,C处红色布条颜色褪去,说明氯气通过D装置后,含有水蒸气,据此即可解答.
解答:解:A.如果D瓶中盛有浓硫酸,浓硫酸具有吸水性,作干燥剂,氯气经过盛有浓硫酸的洗气瓶,为干燥氯气,不能提供水,没有水,就不能生成HClO,就不能使有色布条褪色,故A错误;
B.氯气在饱和食盐水中的溶解度很小,氯气经过饱和食盐水后,氯气与饱和食盐水中的溶剂水反应,生成具有漂白性的HClO,使有色布条褪色,故B正确;
C.氯气经过盛有浓NaOH溶液发生反应:Cl2+2NaOH=NaCl+NaClO+H2O,氯气被吸收,没有气体进入C装置,有色布条不褪色,故C错误;
D.氯气经过盛有NaI溶液发生氧化还原反应:Cl2+2NaI=2NaCl+I2,氯气被吸收,没有气体进入C装置,有色布条不褪色,故D错误;
故选B.
B.氯气在饱和食盐水中的溶解度很小,氯气经过饱和食盐水后,氯气与饱和食盐水中的溶剂水反应,生成具有漂白性的HClO,使有色布条褪色,故B正确;
C.氯气经过盛有浓NaOH溶液发生反应:Cl2+2NaOH=NaCl+NaClO+H2O,氯气被吸收,没有气体进入C装置,有色布条不褪色,故C错误;
D.氯气经过盛有NaI溶液发生氧化还原反应:Cl2+2NaI=2NaCl+I2,氯气被吸收,没有气体进入C装置,有色布条不褪色,故D错误;
故选B.
点评:该题主要考查了氯水能使有色布条褪色的原理,解题时需紧紧抓住干燥氯气不能漂白,潮湿氯气漂白是生成次氯酸,次氯酸具有漂白性这一原理,题目较简单.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案
相关题目
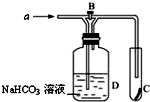 如图所示,从A处通入气体a,若关闭B阀门时,C处有色布条没有明显变化,打开B阀门时,C处有色布条逐渐褪色,则气体a( )
如图所示,从A处通入气体a,若关闭B阀门时,C处有色布条没有明显变化,打开B阀门时,C处有色布条逐渐褪色,则气体a( )| A、肯定是Cl2 | B、肯定是SO2 | C、可能是Cl2和SO2的混合气体 | D、可能是Cl2,也可能是SO2 |
如图所示,从a处通入氯气。若打开活塞b,d处的有色布条不褪色;若关闭活塞b,d处的有色布条褪色。下列判断正确的是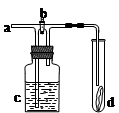
| A.a处通入的是潮湿的氯气 | B.c中盛放的可能是浓硫酸 |
| C.c中盛放的可能是氢氧化钠溶液 | D.c中盛放的可能是饱和食盐水 |
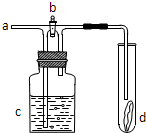 如图所示,从a处通入氯气.若打开活塞b,d处的有色布条不褪色;若关闭活塞b,d处的有色布条褪色.下列判断正确的是( )
如图所示,从a处通入氯气.若打开活塞b,d处的有色布条不褪色;若关闭活塞b,d处的有色布条褪色.下列判断正确的是( ) 如图所示,从A处通入Cl2,关闭B阀门时,C处的红色布条上看不到明显的现象,当打开B阀后,C处红布逐渐褪色,则D瓶中不可能装的是( )
如图所示,从A处通入Cl2,关闭B阀门时,C处的红色布条上看不到明显的现象,当打开B阀后,C处红布逐渐褪色,则D瓶中不可能装的是( )