题目内容
【题目】实验室常用KMnO4和浓盐酸反应制取Cl2,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。则:
(1)氧化剂是________,被氧化的是________。浓盐酸作用______________________,二者物质的量的比值_______________ 。
(2)双线桥分析该氧化还原反应(按照分析标准,注明化合价升降、电子转移数并下定义):____。
【答案】KMnO4 HCl酸及还原剂3:5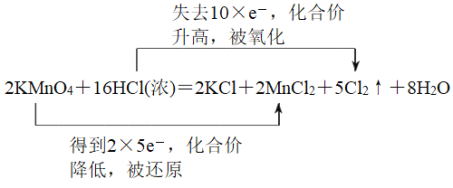
【解析】
(1)反应中Mn元素的化合价从+7价降低到+2价,得到5个电子,发生还原反应,则氧化剂是KMnO4;Cl元素化合价从-1价升高到0价,失去1个电子,发生氧化反应,被氧化的是氯化氢。由于反应中还有氯化锰生成,则浓盐酸的作用是酸及还原剂,根据方程式可知其酸性作用的是6mol,其还原剂作用的是10mol,因此二者物质的量的比值为3:5。
(2)根据以上分析可知用双线桥表示其电子转移的方向和数目为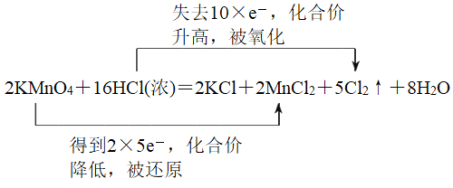 。
。

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目