题目内容
反应N2+3H2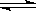 2NH3 ,开始时N2的浓度为3 mol·L-1,H2的浓度为5 mol·L-1,3 min后测得NH3浓度为0.6 mol·L-1,则此时间内,下列反应速率表示正确的是( )
2NH3 ,开始时N2的浓度为3 mol·L-1,H2的浓度为5 mol·L-1,3 min后测得NH3浓度为0.6 mol·L-1,则此时间内,下列反应速率表示正确的是( )
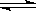 2NH3 ,开始时N2的浓度为3 mol·L-1,H2的浓度为5 mol·L-1,3 min后测得NH3浓度为0.6 mol·L-1,则此时间内,下列反应速率表示正确的是( )
2NH3 ,开始时N2的浓度为3 mol·L-1,H2的浓度为5 mol·L-1,3 min后测得NH3浓度为0.6 mol·L-1,则此时间内,下列反应速率表示正确的是( )| A.v(NH3)=0.2 mol·L-1·s-1 | B.v(N2)=1.0mol·L-1·min-1 |
| C.v(H2)=0.3 mol·L-1·min-1 | D.v(H2)=1.67 mol·L-1·min-1 |
C
试题分析:3 min后测得NH3浓度为0.6 mol·L-1,则用氨气表示的反应速率是0.6 mol/L÷3min=0.2mol·L-1·min-1,A不正确;因为反应速率之比是相应的化学计量数之比,所以氮气和氢气的反应速率分别是0.1mol·L-1·min-1、0.3 mol·L-1·min-1,所以正确的答案选C。
点评:该题是基础性试题的考查,主要是考查学生对反应速率含义以及计算的是熟练掌握程度,难度不大。明确反应速率之比是相应的化学计量数之比是解题的关键,另外还需要注意单位的统一。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 N2(g)+2CO2(g) DH=-a kJ/mol(a>0)
N2(g)+2CO2(g) DH=-a kJ/mol(a>0)
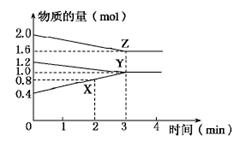
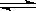 xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,试求:
xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,试求: CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )