题目内容
【题目】把一支试管放在盛有25 ℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5 mL盐酸,回答下列问题:
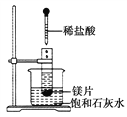
(1)实验中观察到的现象是___________________________________________。
(2)产生上述现象的原因是__________________________________________。
(3)写出有关反应的离子方程式_______________________________________。
【答案】 镁片上有大量气泡产生并逐渐溶解,烧杯中溶液变浑浊 镁与盐酸反应产生氢气,该反应为放热反应,Ca(OH)2在水中的溶解度随温度的升高而减小,故析出Ca(OH)2 Mg+2H+===Mg2++H2↑
【解析】(1)金属镁和盐酸反应产生大量的热,镁片表面冒出气泡,该热量能使氢氧化钙的溶解度降低,所以饱和石灰水变浑浊,故答案为:镁片上有大量气泡产生并逐渐溶解,烧杯中溶液变浑浊;
(2)镁与盐酸反应产生氢气,该反应为放热反应,反应过程中产生大量的热,该热量能使氢氧化钙的溶解度降低,所以饱和石灰水中溶液变浑浊,故答案为:镁与盐酸反应产生氢气,该反应为放热反应,Ca(OH)2在水中的溶解度随温度的升高而减小,故析出Ca(OH)2;
(3)金属镁和盐酸反应的实质是:Mg+2H+═Mg2++H2↑,故答案为:Mg+2H+═Mg2++H2↑。

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目