题目内容
设NA代表阿伏加德罗常数的数值,下列说法中正确的是
- A.标准状况时,22.4L二氯甲烷所含有的分子数为NA
- B.将16gO2与32gSO2在一定的条件下充分反应生成的SO3分子数为NA
- C.碱性锌锰电池中,当有1.3g的锌消耗,则转移的电子数为0.002NA
- D.44g丙烷中含有的非极性共价键数为2NA
D
分析:A、依据气体摩尔体积的条件应用分析,二氯甲烷在标准状况下不是气体分析判断;
B、依据质量关系分析反应的定量关系,关键反应是活性平衡不能进行彻底分析;
C、依据原电池的原理,锌做负极失去电子分析判断;
D、质量换算物质的量,结合丙烷分子结构分析判断,非极性共价键是同元素间形成的共价键;
解答:A、二氯甲烷在标准状况下不是气体,22.4L二氯甲烷不是1mol,分子数不是NA,故A错误;
B、16gO2与32gSO2反应即0.5molO2与0.5molSO2反应,2SO2+O2?2SO3,0.5mol二氧化硫与0.25mol氧气恰好反应生成0.5mol三氧化硫,由于存在化学平衡,实际生成的三氧化硫物质的量小于0.5mol,故B错误;
C、1.3g的锌物质的量=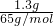 =0.02mol,在原电池反应中的电极反应为Zn-2e-=Zn2+,所以转移的电子数为0.04mol,故C错误;
=0.02mol,在原电池反应中的电极反应为Zn-2e-=Zn2+,所以转移的电子数为0.04mol,故C错误;
D、44g丙烷物质的量= =1mol,根据烷烃分子结构特征,原子间都是形成单键,其中属于非极性共价键的是碳原子间形成,所以,1mol丙烷中三个碳原子形成的非极性共价键数为2NA,故D正确;
=1mol,根据烷烃分子结构特征,原子间都是形成单键,其中属于非极性共价键的是碳原子间形成,所以,1mol丙烷中三个碳原子形成的非极性共价键数为2NA,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常数的应用,主要考查气体摩尔体积的条件应用,化学平衡的应用,原电池的单键反应计算,烷烃结构的分析计算.
分析:A、依据气体摩尔体积的条件应用分析,二氯甲烷在标准状况下不是气体分析判断;
B、依据质量关系分析反应的定量关系,关键反应是活性平衡不能进行彻底分析;
C、依据原电池的原理,锌做负极失去电子分析判断;
D、质量换算物质的量,结合丙烷分子结构分析判断,非极性共价键是同元素间形成的共价键;
解答:A、二氯甲烷在标准状况下不是气体,22.4L二氯甲烷不是1mol,分子数不是NA,故A错误;
B、16gO2与32gSO2反应即0.5molO2与0.5molSO2反应,2SO2+O2?2SO3,0.5mol二氧化硫与0.25mol氧气恰好反应生成0.5mol三氧化硫,由于存在化学平衡,实际生成的三氧化硫物质的量小于0.5mol,故B错误;
C、1.3g的锌物质的量=
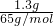 =0.02mol,在原电池反应中的电极反应为Zn-2e-=Zn2+,所以转移的电子数为0.04mol,故C错误;
=0.02mol,在原电池反应中的电极反应为Zn-2e-=Zn2+,所以转移的电子数为0.04mol,故C错误;D、44g丙烷物质的量=
 =1mol,根据烷烃分子结构特征,原子间都是形成单键,其中属于非极性共价键的是碳原子间形成,所以,1mol丙烷中三个碳原子形成的非极性共价键数为2NA,故D正确;
=1mol,根据烷烃分子结构特征,原子间都是形成单键,其中属于非极性共价键的是碳原子间形成,所以,1mol丙烷中三个碳原子形成的非极性共价键数为2NA,故D正确;故选D.
点评:本题考查了阿伏伽德罗常数的应用,主要考查气体摩尔体积的条件应用,化学平衡的应用,原电池的单键反应计算,烷烃结构的分析计算.

练习册系列答案
相关题目