题目内容
在常温常压下,把a mol的NH3和O2的混合气充入密闭容器中,在催化剂存在下加热,使其充分反应,然后恢复到原来的温度和压强.
(1)写出容器内NH3被氧化和形成HNO3的化学方程式.
(2)若原混合气中O2的体积分数为x,最后在容器中生成的HNO3为ymol.
请填写下表.
| x的取值范围 | 用x表示的y值表示式 |
解:(1)氨气在催化剂、加热条件下反应生成一氧化氮和水4NH3+5O2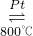 4NO+6H2O;一氧化氮不稳定能和氧气反应生成二氧化氮2NO+O2=2NO2;二氧化氮易和水反应生成硝酸和一氧化氮3NO2+H2O=2HNO3+NO.
4NO+6H2O;一氧化氮不稳定能和氧气反应生成二氧化氮2NO+O2=2NO2;二氧化氮易和水反应生成硝酸和一氧化氮3NO2+H2O=2HNO3+NO.
故答案为:4NH3+5O2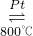 4NO+6H2O; 2NO+O2=2NO2;3NO2+H2O=2HNO3+NO.
4NO+6H2O; 2NO+O2=2NO2;3NO2+H2O=2HNO3+NO.
(2)氧气参加的反应有:4NH3+5O2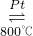 4NO+6H2O; 4NO+3O2+2H2O=4HNO3,所以分三段计算;
4NO+6H2O; 4NO+3O2+2H2O=4HNO3,所以分三段计算;
①当氨气过量氧气不足量或氨气和氧气恰好反应时,根据方程式4NH3+5O2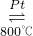 4NO+6H2O知,当0<x
4NO+6H2O知,当0<x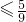 时,没有硝酸生成,所以y=0.
时,没有硝酸生成,所以y=0.
故答案为:0<x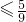 ,y=0.
,y=0.
②当氨气完全反应,氧气过量,过量的氧气恰好与一氧化氮反应时,x的取值范围为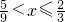 时,生成的硝酸的量为:
时,生成的硝酸的量为:
4NH3+5O2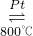 4NO+6H2O;
4NO+6H2O;
4 5
a(1-x)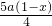
所以与氨气反应消耗氧气的量为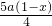 mol,剩余氧气的量为
mol,剩余氧气的量为 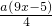 mol,根据剩余氧气的量计算硝酸的物质的量,
mol,根据剩余氧气的量计算硝酸的物质的量,
4 NO+3 O2+2H2O=4 HNO3,
3 4
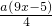 mol ymol
mol ymol
所以y=(3x-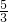 )a
)a
故答案为: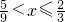 ,y=(3x-
,y=(3x-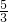 )a.
)a.
③当氧气与一氧化氮反应也过量时,即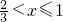 时,生成硝酸的物质的量为ymol,
时,生成硝酸的物质的量为ymol,
4NH3+5O2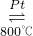 6H2O+4NO;
6H2O+4NO;
4 4
a(1-x)mol a(1-x) mol
生成一氧化氮的物质的量为a(1-x) mol,氧气剩余,所以以一氧化氮的物质的量计算生成硝酸的量.
4 NO+3 O2+2H2O=4 HNO3
4 4
a(1-x) mol ymol
y=a(1-x)
故答案为: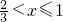 ,y=a(1-x).
,y=a(1-x).
(3)当0<x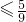 ,y=0
,y=0
当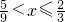 ,y=(3x-
,y=(3x-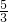 )a.
)a.
当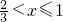 ,y=a(1-x).
,y=a(1-x).
故答案图象如图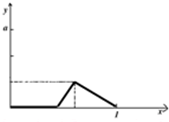 :
:
分析:(1)氨气在催化剂、加热条件下反应生成一氧化氮和水,一氧化氮不稳定能和氧气反应生成二氧化氮,二氧化氮易和水反应生成硝酸和一氧化氮,据此写出相应的反应方程式;
(2)根据氨气和氧气及一氧化氮和氧气的反应方程式进行分段讨论;
(6)根据横坐标和纵坐标之间的关系画出坐标图;
点评:本题以氨气的化学性质为载体考查了有关范围讨论题的计算,难度较大,临界值的准确确定是解本题的关键.
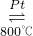 4NO+6H2O;一氧化氮不稳定能和氧气反应生成二氧化氮2NO+O2=2NO2;二氧化氮易和水反应生成硝酸和一氧化氮3NO2+H2O=2HNO3+NO.
4NO+6H2O;一氧化氮不稳定能和氧气反应生成二氧化氮2NO+O2=2NO2;二氧化氮易和水反应生成硝酸和一氧化氮3NO2+H2O=2HNO3+NO.故答案为:4NH3+5O2
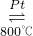 4NO+6H2O; 2NO+O2=2NO2;3NO2+H2O=2HNO3+NO.
4NO+6H2O; 2NO+O2=2NO2;3NO2+H2O=2HNO3+NO.(2)氧气参加的反应有:4NH3+5O2
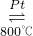 4NO+6H2O; 4NO+3O2+2H2O=4HNO3,所以分三段计算;
4NO+6H2O; 4NO+3O2+2H2O=4HNO3,所以分三段计算;①当氨气过量氧气不足量或氨气和氧气恰好反应时,根据方程式4NH3+5O2
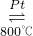 4NO+6H2O知,当0<x
4NO+6H2O知,当0<x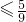 时,没有硝酸生成,所以y=0.
时,没有硝酸生成,所以y=0.故答案为:0<x
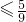 ,y=0.
,y=0.②当氨气完全反应,氧气过量,过量的氧气恰好与一氧化氮反应时,x的取值范围为
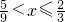 时,生成的硝酸的量为:
时,生成的硝酸的量为:4NH3+5O2
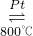 4NO+6H2O;
4NO+6H2O;4 5
a(1-x)
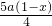
所以与氨气反应消耗氧气的量为
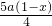 mol,剩余氧气的量为
mol,剩余氧气的量为 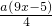 mol,根据剩余氧气的量计算硝酸的物质的量,
mol,根据剩余氧气的量计算硝酸的物质的量,4 NO+3 O2+2H2O=4 HNO3,
3 4
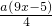 mol ymol
mol ymol所以y=(3x-
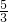 )a
)a故答案为:
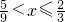 ,y=(3x-
,y=(3x-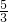 )a.
)a.③当氧气与一氧化氮反应也过量时,即
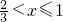 时,生成硝酸的物质的量为ymol,
时,生成硝酸的物质的量为ymol,4NH3+5O2
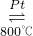 6H2O+4NO;
6H2O+4NO;4 4
a(1-x)mol a(1-x) mol
生成一氧化氮的物质的量为a(1-x) mol,氧气剩余,所以以一氧化氮的物质的量计算生成硝酸的量.
4 NO+3 O2+2H2O=4 HNO3
4 4
a(1-x) mol ymol
y=a(1-x)
故答案为:
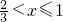 ,y=a(1-x).
,y=a(1-x).| x的取值范围 | 用x表示的y值表达式 |
0<x≤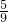 0< 0< | y=0 |
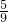 <x≤ <x≤ | y=(3x-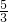 )a )a |
 <x≤1 <x≤1 | y=(1-x)a |
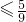 ,y=0
,y=0当
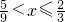 ,y=(3x-
,y=(3x-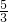 )a.
)a.当
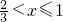 ,y=a(1-x).
,y=a(1-x).故答案图象如图
 :
:分析:(1)氨气在催化剂、加热条件下反应生成一氧化氮和水,一氧化氮不稳定能和氧气反应生成二氧化氮,二氧化氮易和水反应生成硝酸和一氧化氮,据此写出相应的反应方程式;
(2)根据氨气和氧气及一氧化氮和氧气的反应方程式进行分段讨论;
(6)根据横坐标和纵坐标之间的关系画出坐标图;
点评:本题以氨气的化学性质为载体考查了有关范围讨论题的计算,难度较大,临界值的准确确定是解本题的关键.

练习册系列答案
相关题目