题目内容
化学反应C(s)+H2O(g) ![]() CO(g)+H2(g) ΔH>0达到平衡,下列叙述中正确的是 ( )
CO(g)+H2(g) ΔH>0达到平衡,下列叙述中正确的是 ( )
A.升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动
B.加入固体碳,平衡向正反应方向移动
C.加入水蒸气使容器内压强增大,平衡向逆反应方向移动
D.扩大容器容积,平衡向正反应方向移动
D
解析:
升高温度,正、逆速率都增大,故A错误;加入固体碳,没有引起浓度的改变,平衡不移动,故B错误;加入水蒸气使容器内压强增大,只是水蒸气的浓度增大,而一氧化碳和氢气的浓度没有改变,平衡向正反应方向移动,故C错误;扩大容器容积,减小压强,对于C(s)+H2O(g) ![]() CO(g)+H2(g) ΔH>0,正反应方向是体积增大,所以,平衡向正反应方向移动,故D正确。
CO(g)+H2(g) ΔH>0,正反应方向是体积增大,所以,平衡向正反应方向移动,故D正确。

练习册系列答案
相关题目
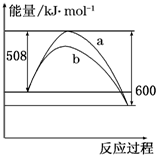 如图是778K时氮气与氢气合成氨反应过程中能量变化的曲线图,下列叙述正确的是( )
如图是778K时氮气与氢气合成氨反应过程中能量变化的曲线图,下列叙述正确的是( )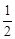 O2(g)==CO(g);△H= — Q1 kJ/mol,
O2(g)==CO(g);△H= — Q1 kJ/mol,