题目内容
(2012?房山区二模)常温下,下列关于电解质溶液的叙述中不正确的是( )
分析:A.根据电荷守恒判断;
B.等物质的量浓度、等体积的醋酸溶液与氢氧化钠溶液恰好反应生成醋酸钠,根据盐的类型确定溶液的酸碱性;
C.氢离子抑制铵根离子水解,碳酸氢根离子促进铵根离子水解;
D.酸或碱抑制水电离,含有弱根离子的盐促进水电离.
B.等物质的量浓度、等体积的醋酸溶液与氢氧化钠溶液恰好反应生成醋酸钠,根据盐的类型确定溶液的酸碱性;
C.氢离子抑制铵根离子水解,碳酸氢根离子促进铵根离子水解;
D.酸或碱抑制水电离,含有弱根离子的盐促进水电离.
解答:解:A.溶液呈电中性,溶液中阴阳离子所带电荷相等,根据电荷守恒得c(H+)+c(NH4+)=c(Cl-)+c(OH-),故A正确;
B.等物质的量浓度、等体积的醋酸溶液与氢氧化钠溶液恰好反应生成醋酸钠,醋酸钠是强碱弱酸盐,其溶液呈碱性,故B错误;
C.硫酸氢铵能电离出氢离子,氢离子抑制铵根离子水解,碳酸氢铵中碳酸氢根离子和铵根离子相互促进水解,所以等物质的量浓度的NH4HSO4、NH4HCO3溶液中c(NH4+)大小,NH4HSO4>NH4HCO3,故C正确;
D.酸或碱抑制水电离,含有弱根离子的盐促进水电离,所以醋酸抑制水电离,醋酸钠促进水电离,则等物质的量浓度的醋酸与醋酸钠溶液中水电离产生的c(OH-),前者小于后者,故D正确;
故选B.
B.等物质的量浓度、等体积的醋酸溶液与氢氧化钠溶液恰好反应生成醋酸钠,醋酸钠是强碱弱酸盐,其溶液呈碱性,故B错误;
C.硫酸氢铵能电离出氢离子,氢离子抑制铵根离子水解,碳酸氢铵中碳酸氢根离子和铵根离子相互促进水解,所以等物质的量浓度的NH4HSO4、NH4HCO3溶液中c(NH4+)大小,NH4HSO4>NH4HCO3,故C正确;
D.酸或碱抑制水电离,含有弱根离子的盐促进水电离,所以醋酸抑制水电离,醋酸钠促进水电离,则等物质的量浓度的醋酸与醋酸钠溶液中水电离产生的c(OH-),前者小于后者,故D正确;
故选B.
点评:本题考查酸碱混合溶液定性判断、盐类水解、弱电解质的电离等知识点,易错选项是C,注意:在水溶液中硫酸氢铵和碳酸氢铵电离方程式的区别,为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
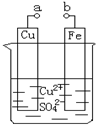 (2012?房山区二模)某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
(2012?房山区二模)某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )