题目内容
X、Y、Z、Q、E五种元素中,X原子核外的M层中有2个单电子且与Z同主族,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大.请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)YZ2分子的立体结构是 ;
(3)Q的元素符号是 ,它的核外电子排布式为 ,在形成化合物时它的最高化合价为 ;
(4)E的氢化物的熔沸点比同族其它元素氢化物的熔沸点都要高很多,原因是 HF分子间存在
.
考点: 位置结构性质的相互关系应用.
分析: Y原子核外的L层电子数是K层的两倍,Y有2个电子层,最外层电子数为4,故Y为C元素;X原子核外的M层中有2个单电子且与Z同主族,则X为S元素;Z是地壳内含量最高的元素,则Z为O元素;Q的核电荷数是X与Z的核电荷数之和,原子序数为24,为Cr元素,E在元素周期表的各元素中电负性最大,应为F元素,结合元素对应单质、化合物的结构和性质解答该题.
解答: 解:Y原子核外的L层电子数是K层的两倍,Y有2个电子层,最外层电子数为4,故Y为C元素;X原子核外的M层中有2个单电子且与Z同主族,则X为S元素;Z是地壳内含量最高的元素,则Z为O元素;Q的核电荷数是X与Z的核电荷数之和,原子序数为24,为Cr元素,E在元素周期表的各元素中电负性最大,应为F元素,
(1)由以上分析可知,X为S,Y为C,
故答案为:S;C;
(2)YZ2分子为CO2,C和O形成2个δ键,没有孤电子对,为直线型,
故答案为:直线型;
(3)Q为Cr,原子序数为24,位于周期表第四周期ⅥB族,核外电子排布式为:s22s22p63s23p63d54s1,最高化合价为+6价,
故答案为:Cr;1s22s22p63s23p63d54s1;+6;
(4)E为F元素,由于HF分子间存在氢键,则HF的熔沸点比同族其它元素氢化物的熔沸点都要高很多,
故答案为:HF分子间存在氢键.
点评: 本题考查位置、结构与性质关系的综合应用,题目难度中等,本题注意把握原子核外电子排布,推断元素的种类是关键,还要注意把握分析空间构型的判断.

 O2(g)=CO2(g))△H=﹣Q1kJ/mol;
O2(g)=CO2(g))△H=﹣Q1kJ/mol;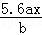 B.
B. 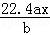 C.
C. 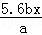 D.
D.