题目内容
【题目】将0.1mol的镁、铝混合物溶于100mL2mol/LH2SO4溶液中,然后再滴加1mol/LNaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.当V2=460mL时,则原混合物中镁铝的质量比是( ) 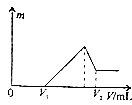
A.1:1
B.2:3
C.16:27
D.8:9
【答案】C
【解析】解:当V2=460mL时,溶液的组成是NaAlO2和Na2SO4混合液,在硫酸钠中,n(SO ![]() )=0.5n(Na+)=0.2mol,所以硫酸钠中钠离子物质的量是0.4mol,根据钠守恒,所以n(NaAlO2)=n(Al)=0.46L×1mol/L﹣0.4mol=0.06mol,所以镁的物质的量是0.04mol,原混合物中镁铝的质量比是
)=0.5n(Na+)=0.2mol,所以硫酸钠中钠离子物质的量是0.4mol,根据钠守恒,所以n(NaAlO2)=n(Al)=0.46L×1mol/L﹣0.4mol=0.06mol,所以镁的物质的量是0.04mol,原混合物中镁铝的质量比是 ![]() =
= ![]() ,故选C.
,故选C.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】相同体积的某营养液两份,其配方如下表:
KCl | K2SO4 | ZnSO4 | ZnCl2 | |
(1) | 0.3mol | 0.2mol | 0.1mol | ╱ |
(2) | 0.1mol | 0.3mol | ╱ | 0.1mol |
比较两份营养液中各种离子的浓度,下列有关说法正确的是( )
A.各种离子的浓度均相同
B.只有c(K+)相同
C.各种离子的浓度均不同
D.只有c(Zn2+)相同