题目内容
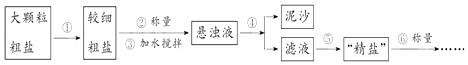
【题目】常温下,将除去表面氧化膜的A1、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示。反应过程中有红棕色气体产生。下列说法错误的是 ( )
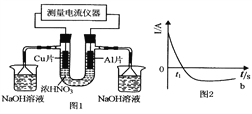
A. t1时刻前,A1片的电极反应为:2A1+3H2O - 6e- ═ A12O3+6H+
B. t1时,因A1在浓硝酸中钝化,氧化膜阻碍了A1继续反应
C. t1之后,负极Cu失电子,电流方向发生改变
D. 烧杯中发生的离子反应为:2NO2+2OH- ═ 2NO3-+H2O
【答案】D
【解析】A.t1时刻前,铝片做负极反应,Al发生氧化反应,负极发生2A1-6e-+3H2O===A12O3+6H+,故A正确;B.t1时,随着反应进行铝表面钝化形成氧化膜阻碍反应进行,故B正确;C.随着反应进行铝表面钝化形成氧化膜阻碍反应进行,铜做负极反应,电流方向相反,故C正确;D. NO2溶解于NaOH溶液生成NaNO3和NaNO2,烧杯中发生的离子反应为:2NO2+2OH-=NO3-+NO2-+H2O,故D错误;答案为D。

 阅读快车系列答案
阅读快车系列答案【题目】研究人员为了比较甲、乙、丙三种微生物所产生的淀粉酶(提取液中酶蛋白浓度相同)的活性,进行了如下实验:
分组试剂(mL) | 试管1 | 试管2 | 试管3 | 试管4 |
蒸馏水 | 2 | 2 | 2 | A |
pH=8缓冲液 | 0.5 | 0.5 | 0.5 | 0.5 |
淀粉溶液 | 1 | 1 | 1 | 1 |
甲生物提取液 | 0.3 | |||
乙生物提取液 | 0.3 | |||
丙生物提取液 | 0.3 | |||
总体积 | 3.8 | 3.8 | 3.8 | B |
结果如下表(注:“+”显色,“++”显色更深;“﹣”不显色),请分析回答下列问题:
试管1 | 试管2 | 试管3 | 试管4 | |
颜色深浅程 | ++ | ﹣ | + | C |
(1)表中A的数值为 ,C的颜色深浅程度 (用“+“或“﹣”表示).
(2)该实验的自变量是 ,无关变量有 (写出2种即可).
(3)除了用碘液检验淀粉的剩余量来判断实验结果外,还可以用 试剂来检测生成物的量.若用该试剂检验,颜色变化最深的试管是 .
(4)根据上述结果得出的结论是:不同来源的淀粉酶,虽然酶蛋白浓度相同,但活性不同.造成实验中三种酶活性差异的根本原因是 .
(5)同学们还做了反应速率与底物浓度关系的实验.右上坐标中已根据实验结果画出3号试管中酶活性的曲线,请你在坐标中画出2号试管中酶活性的曲线. .