题目内容
选做试题,考生可从A、B两小题中任选一题进行解答,若两题均做,则以A题为准。A.Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据列于下表:
元素 | Mn | Fe | |
电离能/kJ·mol-1 | I1 | 717 | 759 |
I2 | 1 509 | 1 561 | |
I3 | 3 248 | 2 957 | |
回答下列问题:
(1)Mn元素价电子层的电子排布式为_____________,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。对此,你的解释是____________________。
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是________________________。
(3)三氯化铁常温下为固体,熔点
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如下图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为____________。

B.有机化合物A的分子式是C13H20O8(相对分子质量为304),1 mol A在酸性条件下水解得到4 mol CH3COOH和1 mol B。B分子结构中每一个连有羟基的碳原子上还连有两个氢原子。
请回答下列问题:
(1)A和B的相对分子质量之差是____________。
(2)B的结构简式是_________________。
(3)B能发生的反应是___________(填写序号)。
①氧化反应 ②取代反应 ③消去反应 ④缩聚反应
(4)已知:

以两种一元醛(其物质的量之比为1∶4)和必要的无机试剂为原料合成B,写出合成B的各步反应的化学方程式。
A.(1)3d54s2 由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态(或Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态)
(2)具有孤对电子 (3)分子 (4)2∶1
解析:(2)可以利用教材知识直接得出,(3)是利用晶体性质对晶体类型的判定,比较简单;(4)是对晶体中原子分摊的考查,在面心立方中,铁原子数为8×1/8+6×1/2=4个,体心立方中铁原子数为8×1/8+1=2个,所以个数比为2∶1。
B.(1)168 (2)C(CH2OH)4
(3)①②④
(4)CH3CHO+3HCHO![]() (CH2OH)3CCHO
(CH2OH)3CCHO
(CH2OH)3CCHO+HCHO+NaOH(浓)![]() C(CH2OH)4+HCOONa
C(CH2OH)4+HCOONa
解析:在解析时要注意,1 mol A在酸性条件下水解得到4 mol乙酸和1 mol B,则B分子中含有4个羟基,又因为B分子结构中每一个连有羟基的碳原子上还连有两个氢原子,不难得出B的结构,从而顺利得出(1)(2)(3)的答案;(4)题中可以利用信息,得出两种醛分别为乙醛和甲醛,然后得出答案。

 孟建平名校考卷系列答案
孟建平名校考卷系列答案 的沸点高于
的沸点高于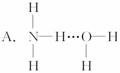

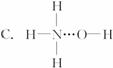

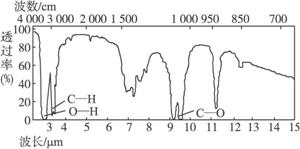
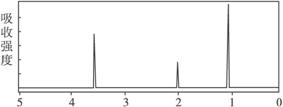
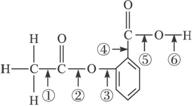
 ),请写出“502胶”发生黏合作用的化学方程式:_____________________________;反应类型是_____________。
),请写出“502胶”发生黏合作用的化学方程式:_____________________________;反应类型是_____________。 )也是一种黏合剂,工业上用丙烯酸和某物质在一定条件下反应可制得这种黏合剂,该物质的名称是_____________;请写出这一制取过程的化学方程式_________________。
)也是一种黏合剂,工业上用丙烯酸和某物质在一定条件下反应可制得这种黏合剂,该物质的名称是_____________;请写出这一制取过程的化学方程式_________________。 、
、 、
、 。已知含有
。已知含有