题目内容
3.(1)实验室制备氢氧化铁胶体化学方程式:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl.(2)能证明Na2SO3溶液中存在SO32-+H2O?HSO3-+OH-水解平衡的事实是C(填选项字母).
A.滴入酚酞溶液变红,再加入H2SO4溶液后红色退去
B.滴入酚酞溶液变红,再加入氯水后红色退去
C.滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去
(3)现有可逆反应:2A(g)+2B(g)?C(g)+3D(s),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:Ⅰ.A、B的起始物质的量均为2mol,Ⅱ.C、D的起始物质的量分别为2mol和6mol.以下说法中正确的是C(填选项字母).
A.Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的百分组成相同
B.达到平衡时,途径Ⅱ所得混合气密度为途径Ⅰ所得混合气密度的2倍
C.达到平衡时,途径Ⅱ中C的平衡浓度大于途径Ⅰ中C的平衡浓度的2倍
(4)在恒容绝热(不与外界交换能量)条件下进行2A (g)+B(g)?2C(g)+D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高.简述该反应的平衡常数与温度的变化关系:该反应的平衡常数K随温度的升高而减小.
| 物质 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |
分析 (1)氯化铁在沸水中水解生成胶体;
(2)利用平衡移动证明Na2SO3溶液中存在SO32-+H2O?HSO3-+OH-水解平衡;
(3)在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:Ⅰ.A、B的起始物质的量均为2mol,Ⅱ.C、D的起始物质的量分别为2mol和6mol,对于途径II极性转化为A、B,A、B的起始物质的量均为4mol.二者为等效平衡,二者为等效平衡,但D为固体,II中压强大,平衡正向移动;
(4)2A (g)+B(g)?2C(g)+D(s)反应,反应为气体体积缩小的反应,容器的体积不变,平衡时压强增大,故绝热条件下,混合气体的温度升高,即正反应为放热反应,结合温度对平衡移动的影响判断温度与平衡常数的变化关系.
解答 解;(1)实验室制备氢氧化铁胶体的方法是:加热烧杯中的水至沸腾,向沸水滴加几滴饱和氯化铁溶液,继续煮沸至溶液呈红褐色,即停止加热,要注意实验过程不能用玻璃棒搅拌,否则溶液出现浑浊;当反应体系呈现红褐色,即制得氢氧化铁胶体,应立即停止加热,否则也容易出现浑浊,产生红褐色的氢氧化铁沉淀,往沸水中滴加饱和氯化铁溶液后,可稍微加热煮沸,但不宜长时间加热,反应原理为:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl,
故答案为:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;
(2)A.滴入酚酞溶液变红,再加入H2SO4溶液后反应生成硫酸钠、水和二氧化硫,不能确定水解平衡的存在,故A不选;
B.滴入酚酞溶液变红,再加入氯水后,发生氧化还原反应,生成硫酸钠,且氯水中HClO具有漂白性,不能确定水解平衡的存在,故B不选;
C.滴入酚酞溶液变红,再加入BaCl2溶液后,SO32-+H2O?HSO3-+OH-水解平衡逆向移动,产生沉淀且红色褪去,故C选;
故答案为:C;
(3)在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:Ⅰ.A、B的起始物质的量均为2mol,Ⅱ.C、D的起始物质的量分别为2mol和6mol,对于途径II极性转化为A、B,A、B的起始物质的量均为4mol,二者为等效平衡,但D为固体,II中压强大,平衡正向移动,则
A.Ⅰ、Ⅱ两条途径最终达到的平衡为等效平衡,II中压强大,平衡正向移动的趋势大,则体系内各混合气体的百分组成不相同,故A错误;
B.达到平衡时,D为固体,Ⅱ中气体的总质量小于Ⅰ的2倍,而容器容积相同,即途径Ⅱ所得混合气密度小于途径Ⅰ所得混合气密度的2倍,故B错误;
C.达到平衡时,两个平衡为等效平衡,由于Ⅱ中初始反应物为Ⅰ的2倍,II中压强大,生成C大于I中额的2倍,且容器容积相同,达到平衡时,途径ⅡC的平衡浓度大于途径ⅠC的平衡浓度的2倍,故C正确;
故答案为:C;
(4)由起始D的物质的量为0可知,反应2A (g)+B(g)?2C(g)+D(s)向正反应进行建立平衡,正反应是气体体积减小的反应,容器的体积不变,平衡时压强增大,故绝热条件下,混合气体的温度升高,即正反应为放热反应,升高温度平衡向逆反应进行,化学平衡常数减小,
故答案为:该反应的平衡常数K随温度的升高而减小.
点评 本题考查较综合,涉及化学平衡常熟的含有、平衡移动、等效平衡及盐类水解等,注重高频考点的考查,(3)中注意D为固体为解答的易错点,综合性较强,题目难度中等.

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案方案Ⅰ:铜铝混合物
| 足量溶液A |
| 充分反应 |
方案Ⅱ:铜铝混合物
| 足量溶液B |
| 充分反应 |
下列有关判断中不正确的是( )
| A. | 溶液A和B均可以是盐酸 | B. | 溶液A和B均可以是NaOH溶液 | ||
| C. | 溶液A和B均可选用稀硝酸 | D. | 实验室中方案Ⅱ更便于实施 |
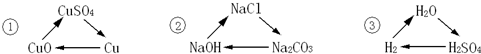
| A. | ①和② | B. | ②和③ | C. | ①和③ | D. | ①②③ |
| A. | 滤纸上有Ag,Cu,Fe滤液中有Fe2+,Mg2+ | |
| B. | 滤纸上有Ag,滤液中有Fe2+,Cu2+,Mg2+,Ag+ | |
| C. | 滤纸上有Ag,Cu,滤液中有Fe2+,Cu2+,Mg2+ | |
| D. | 滤纸上有Ag,Cu,滤液中有Fe2+,Cu2+,Mg2+,Ag+ |
| A. | 若a1=a2,b1=b2,则混合溶液中c(CH3COO-)=c(Na+)>c(H+)=c(OH-) | |
| B. | 若a1=a2,b1=2b2,则混合溶液中c(CH3COO-)>c(CH3COOH)>c(Na+) | |
| C. | 若a1b1>a2b2,则混合液的pH一定大于7 | |
| D. | a1=a2,且混合溶液的pH<7,则b1一定大于b2 |

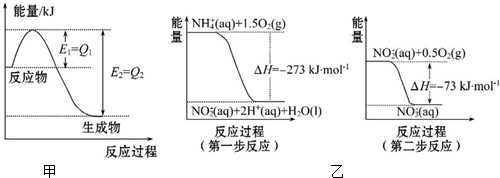
 A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,它们之间的转化关系如图所示((图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).
A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,它们之间的转化关系如图所示((图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).