题目内容
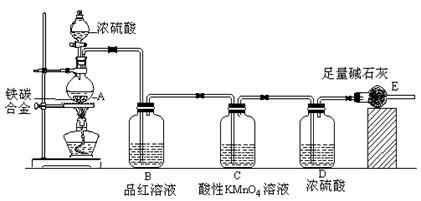
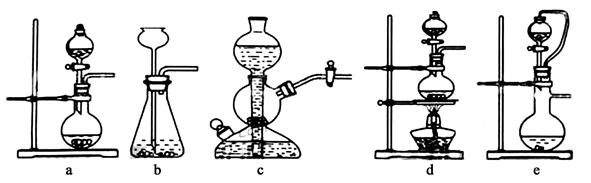
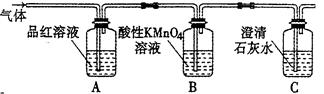
现有某铁碳合金(铁和碳两种单质的混合物),某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究。

I.测定铁的质量分数:
(1)检查上述装置气密性的一种方法是:关闭分液漏斗的活塞,在E装置后面连上一根
导管,然后________________________________________,则证明装置的气密性良好。
(2)称量E的质量,并将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg。铁碳合金中铁的质量分数为_____________________________________________(写表达式)。
(3)装置C中反应的离子方程式为________________________________________。
(4)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,原因是空气中CO2、H2O进入E管使b增大。你认为改进的方法是____________________________________.
(5)乙同学认为,即使甲同学认为的偏差得到改进,依据此实验测得合金中铁的质量分
数也可能会偏离。你认为其中的原因是_________________________________________。
Ⅱ.探究浓硫酸的某些性质:
(6)往A中滴加足量的滚硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:
_____________________________________________________________________。
(7)将A中固体换为金属铜则与浓硫酸发生反应的化学方程式是__________________
_______________________,反应中浓硫酸表现出的性质是______________________。

I.测定铁的质量分数:
(1)检查上述装置气密性的一种方法是:关闭分液漏斗的活塞,在E装置后面连上一根
导管,然后________________________________________,则证明装置的气密性良好。
(2)称量E的质量,并将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg。铁碳合金中铁的质量分数为_____________________________________________(写表达式)。
(3)装置C中反应的离子方程式为________________________________________。
(4)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,原因是空气中CO2、H2O进入E管使b增大。你认为改进的方法是____________________________________.
(5)乙同学认为,即使甲同学认为的偏差得到改进,依据此实验测得合金中铁的质量分
数也可能会偏离。你认为其中的原因是_________________________________________。
Ⅱ.探究浓硫酸的某些性质:
(6)往A中滴加足量的滚硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:
_____________________________________________________________________。
(7)将A中固体换为金属铜则与浓硫酸发生反应的化学方程式是__________________
_______________________,反应中浓硫酸表现出的性质是______________________。
(1)把导管放入盛水的水槽中,微热烧瓶,如果导管口有气泡产生,停止加热后导管口产生一段稳定的水柱。(2分)
(2)(11a-3b)/11a×100℅(2分)
(3)2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+(2分)
(4)在装置E的后边再连接一个与E相同的装置。(2分)
(5)反应产生的CO2气体未能完全排到装置E中,导致b偏低。
(6)常温下,铁被浓硫酸钝化,碳不与浓硫酸反应。(2分)
(7) 2H2SO4(浓)+Cu
 CuSO2+ SO2↑+2H2O; (2分) 酸性和强氧化性(2分)
CuSO2+ SO2↑+2H2O; (2分) 酸性和强氧化性(2分)试题分析:(1)用微热法检验密封装置的气密性。
(2)E增重bg,是CO2的质量,可以计算碳的质量3b/11g,铁的质量 (a-3b/11)g, 铁的质量分数为(11a-3b)/11a×100℅.
(3)装置C中是K MnO4溶液,有强氧化性,能和有还原性的SO2反应,离子方程式为2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+。
(4)为防止空气中CO2、H2O进入E管,可以在E的后边再连接一个与E相同的装置,吸收空气中CO2、H2O。
(5)反应结束后,装置内还有生成的气体残留。
(6) 常温下,铁被浓硫酸钝化,碳不与浓硫酸反应。
(7) 铜与浓硫酸加热的条件下发生反应,生成CuSO2和 SO2。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
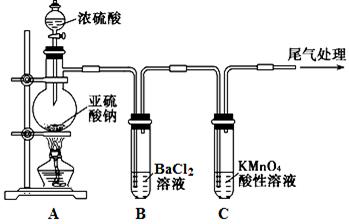
 Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
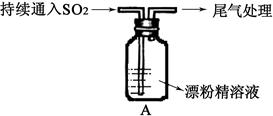
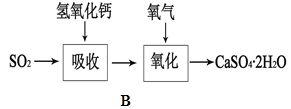
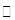 CO2↑+2SO2↑+2H2O,其中浓H2 S04所起的作用是 (填“氧化剂”或“还原剂”)。若有0.2mol碳的完全反应,则消耗H2S04的质量是 g,标况下产生SO2的体积为______________L。
CO2↑+2SO2↑+2H2O,其中浓H2 S04所起的作用是 (填“氧化剂”或“还原剂”)。若有0.2mol碳的完全反应,则消耗H2S04的质量是 g,标况下产生SO2的体积为______________L。