题目内容
化学必修一教材47页3-2实验演示的是钠与氧气的反应,实验操作及现象如下(1)从______中用______取一小块钠,用小刀切开.
(2)把一小块金属钠放在______里,加热时,钠先熔化为银白色的小球,然后燃烧.火焰呈______色.最后生成______色固体.
(3)该实验所涉及的方程式为:______ Na2O2
【答案】分析:(1)钠性质较活泼,能和氧气、水反应,为了防止钠变质,要密封保存;
(2)钠在坩埚里燃烧发出黄色火焰,生成淡黄色的固体;
(3)根据反应物和生成物,写出钠和氧气反应的方程式;
(4)根据钠和水反应的反应物、生成物及离子方程式的书写规则写出相应的离子方程式,铝是一种特殊的金属,既能与强酸反应又能与强碱反应.
解答:解:(1)钠性质较活泼,能和氧气、水反应,且钠的密度小于水而大于煤油,所以用煤油保存钠,钠和水反应生成的氢氧化钠具有强腐蚀性,所以从煤油中用镊子取钠,
故答案为:煤油;镊子;
(2)用于灼烧固体的仪器是坩埚,所以用坩埚灼烧钠,钠燃烧生成淡黄色的过氧化钠,且同时发出黄色火焰,故答案为:坩埚;黄色;淡黄色;
(3)钠在空气中燃烧生成淡黄色固体过氧化钠,反应方程式为:2Na+O2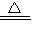 Na2O2,故答案为:2Na+O2
Na2O2,故答案为:2Na+O2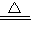 Na2O2;
Na2O2;
(4)钠和水反应生成氢氧化钠和氢气,离子反应方程式为2Na+2H2O=2Na++2OH-+H2↑,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,离子反应方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评:本题考查钠的性质,明确钠和水、氧气的反应即可解答,注意焰色反应是元素的性质.
(2)钠在坩埚里燃烧发出黄色火焰,生成淡黄色的固体;
(3)根据反应物和生成物,写出钠和氧气反应的方程式;
(4)根据钠和水反应的反应物、生成物及离子方程式的书写规则写出相应的离子方程式,铝是一种特殊的金属,既能与强酸反应又能与强碱反应.
解答:解:(1)钠性质较活泼,能和氧气、水反应,且钠的密度小于水而大于煤油,所以用煤油保存钠,钠和水反应生成的氢氧化钠具有强腐蚀性,所以从煤油中用镊子取钠,
故答案为:煤油;镊子;
(2)用于灼烧固体的仪器是坩埚,所以用坩埚灼烧钠,钠燃烧生成淡黄色的过氧化钠,且同时发出黄色火焰,故答案为:坩埚;黄色;淡黄色;
(3)钠在空气中燃烧生成淡黄色固体过氧化钠,反应方程式为:2Na+O2
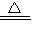 Na2O2,故答案为:2Na+O2
Na2O2,故答案为:2Na+O2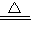 Na2O2;
Na2O2;(4)钠和水反应生成氢氧化钠和氢气,离子反应方程式为2Na+2H2O=2Na++2OH-+H2↑,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,离子反应方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评:本题考查钠的性质,明确钠和水、氧气的反应即可解答,注意焰色反应是元素的性质.

练习册系列答案
相关题目