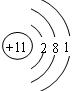
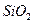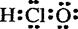题目内容
向硫酸铜溶液中通入足量NH3后可得到深蓝色溶液[溶质为Cu(NH3)4SO4],再向所得溶液通入SO2至溶液呈微酸性发现有白色沉淀Q生成,反应方程式为:①2Cu(NH3)4SO4+3SO2+4H2O=
2NH4CuSO3↓+3(NH4)2SO4。再将Q与足量的10mol/L硫酸混合微热,则会发生如下反应:②2NH4CuSO3+2H2SO4=Cu+(NH4)2SO4+2SO2+CuSO4+2H2O。下面有关分析中正确的是
2NH4CuSO3↓+3(NH4)2SO4。再将Q与足量的10mol/L硫酸混合微热,则会发生如下反应:②2NH4CuSO3+2H2SO4=Cu+(NH4)2SO4+2SO2+CuSO4+2H2O。下面有关分析中正确的是
| A.①是非氧化还原反应,而②是氧化还原反应 |
| B.上述反应中SO2的作用只相当于催化剂 |
| C.反应②中CuSO4是氧化产物 |
| D.反应①中SO2发生还原反应 |
C
略

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
 气同时通入水中反应的化学方程式:
气同时通入水中反应的化学方程式: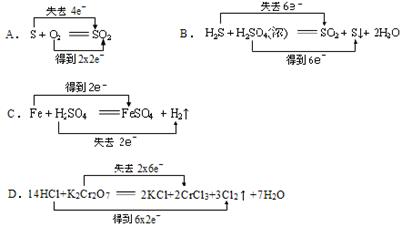
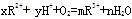 的离子方程式中,对系数m和R2+、R3+判断正确的是
的离子方程式中,对系数m和R2+、R3+判断正确的是