题目内容
下列有关说法和结论都正确的是
A.已知 = = ,氢气还原氧化铜后所得红色固体能完全溶于稀硝酸,说明红色固体是铜 ,氢气还原氧化铜后所得红色固体能完全溶于稀硝酸,说明红色固体是铜 |
B.用蒸馏水、酚酞、 溶液和已知浓度盐酸标准溶液作试剂,可测定NaOH固体(杂质仅为 溶液和已知浓度盐酸标准溶液作试剂,可测定NaOH固体(杂质仅为 )的纯度 )的纯度 |
C.将 气体通入溴水中,溴水颜色逐渐褪去,说明 气体通入溴水中,溴水颜色逐渐褪去,说明 具有漂白性 具有漂白性 |
D.已知 的溶解度小于 的溶解度小于 |
B
解析试题分析:A、Cu2O能与HNO3反应,溶于硝酸,所以氢气还原氧化铜后所得红色固体能完全溶于稀硝酸,红色固体可能是铜,也可能含Cu2O,错误;B、加入BaCl2溶液可除去杂质Na2CO3,然后用盐酸标准溶液滴定,可测定NaOH固体的纯度,正确;C、将SO2气体通入溴水中,溴水颜色逐渐褪去,Br2氧化SO2,体现了SO2的还原性,错误;D、Ag2CrO4与AgCl的化学式组成不同,所以不能直接根据Ksp的大小判断溶解度的大小,错误。
考点:本题考查物质的性质、Ksp与溶解度的关系。

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
下列实验现象可用同一原理解释的是
| A.品红溶液中分别通入SO2和Cl2,品红均褪色 |
| B.溴水分别滴入植物油和裂化汽油中,溴水均褪色 |
| C.鸡蛋白溶液中分别加入NaCl溶液和HgCl2溶液,均有固体析出 |
| D.分别加热盛有NH4Cl和单质碘的试管,管口均有固体凝结 |
一定量的浓硝酸与过量的铜充分反应,生成的气体是
| A.只有NO2 | B.只有NO | C.NO2和H2 | D.NO2和NO |
下列有关说法,不正确的是
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②酒精灯加热铝箔至熔化,铝并不滴落,因为铝表面的一层致密氧化膜熔点比铝高
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④将硅酸钠浸透的滤纸在酒精灯上灼烧,因为是湿滤纸温度低所以不能燃烧
| A.①③④ | B.②③④ | C.①③ | D.①②④ |
下列实验现象描述正确的是
| A.HCl与NH3相遇有大量的白烟生成 |
| B.用洁净玻棒蘸取Na2SO4溶液灼烧火焰呈紫色 |
| C.FeCl2溶液与无色的KSCN溶液混合,溶液呈红色 |
| D.SO2通入品红溶液,红色褪去,再加热,红色不再出现 |
甲、乙、丙、丁是中学常见的物质,其中甲、乙、丙均含有同一种元素,在一定条件下的转化关系如图,下列说法正确的是
| A.若丁为用量最大,用途最广的金属单质,乙的溶液一定为FeCl3 |
B.若通常情况下甲、乙、丙、丁都是气体,且乙和丁为空气的主要成分,则反应①的化学方程式4NH3+5O2 4NO+6H2O 4NO+6H2O |
| C.若甲、乙、丙的溶液显碱性,丙可作为医疗上治疗胃酸过多症的药剂,将等物质的量的乙和丙溶于水形成混合溶液,溶液中各离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)> c(H+) |
| D.若丁为化合物,且为氯碱工业的重要产品,则甲一定为含Al3+的盐 |
下表所列各组物质中,物质之间通过一步反应不能实现如下图所示转化的是( )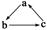
| 选项 | a | b | c |
| A | Fe | FeCl3 | FeCl2 |
| B | Al(OH)3 | NaAlO2 | Al2O3 |
| C | HNO3 | NO | NO2 |
| D | CH2=CH2 | CH3CH2Br | CH3CH2OH |
下表中除去杂质应选用的试剂或操作方法正确的是( )
| 选项 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| A | KNO3溶液 | KOH | 加入FeCl3溶液,并过滤 |
| B | FeCl3溶液 | FeCl2 | 加入稍过量双氧水后放置 |
| C | CO | O2 | 通过灼热的铜网后收集气体 |
| D | K2CO3固体 | NaHCO3 | 置于坩埚中加热 |
可用如图所示装置制取、净化、收集的气体是( )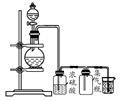
| A.锌和稀硝酸反应制一氧化氮 |
| B.亚硫酸钠与浓硫酸反应制二氧化硫 |
| C.铁和稀硫酸反应制氢气 |
| D.浓氨水和生石灰反应制取氨气 |