题目内容
合成氨原料可以由天然气制取。其主要反应为:CH4(g)+H2O(g)(1)1 m3(标准状况)CH4按上式完全反应,产生H2___________mol。
(2)CH4和O2的反应为:2CH4(g)+O2(g)![]() 2CO(g)+4H2(g),设CH4同时和H2O(g)及O2(g)反应。1 m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为_____________。
2CO(g)+4H2(g),设CH4同时和H2O(g)及O2(g)反应。1 m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为_____________。
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
气体 | CO | H2 | N2 | O2 |
体积(L) | 24 | 60 | 15 | 2.5 |
计算该富氧空气中O2和N2的体积比V(O2)/V(N2)。
(4)若CH4和H2O(g)及富氧空气混合反应的产物中,V(H2)∶V(N2)=3∶1(合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为何值?
解析:(1)设1 m3 CH4完全反应可产生H2、CO的物质的量分别为x、y,则
CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
1 mol 1 mol 3 mol
![]() y x
y x
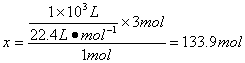
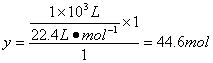 。
。
(2)由反应CH4(g)+H2O(g)![]() CO(g)+3H2(g)知,1 m3标况下的CH4,产生气体的体积为4 m3;而1 m3 CH4在标况下按反应2CH4(g)+O2(g)
CO(g)+3H2(g)知,1 m3标况下的CH4,产生气体的体积为4 m3;而1 m3 CH4在标况下按反应2CH4(g)+O2(g) ![]() 2CO(g)+4H2(g)进行时产生气体的体积为3 m3,故1 m3 CH4同时按上述两种反应进行时产生气体的体积应介于3 m3与4 m3之间。
2CO(g)+4H2(g)进行时产生气体的体积为3 m3,故1 m3 CH4同时按上述两种反应进行时产生气体的体积应介于3 m3与4 m3之间。
(3)设参加反应的H2O的体积为x,O2的体积为y,由:
CH4(g)+H2O(g) ![]() CO(g)+3H2(g)
CO(g)+3H2(g)
1 1 3
X V(CO) V(H2)
V(CO)=x V(H2)=3x
又2CH4(g)+O2(g) ![]() 2CO(g)+4H2(g)
2CO(g)+4H2(g)
1 2 4
y V′(CO) V′(H2)
V′(CO)=y V′(H2)=4y
则![]()
所以![]() 。
。
(4)设富氧空气中O2的体积分数为a,反应用去的H2O(g)与富氧空气的体积分别为x、y,则
CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
x 3x
2CH4(g)+O2(g) ![]() 2CO(g)+4H2(g)
2CO(g)+4H2(g)
y·a 4ay
所以有![]()
![]()
答案:(1)133.9 (2)3 m3<V<4 m3 (3)V(O2)/V(N2)=![]() (4)V[H2O(g)]∶V(空气)=1-
(4)V[H2O(g)]∶V(空气)=1-![]() a
a

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
(1)1 m3(标准状况)CH4按上式完全反应,产生H2________________mol。
(2)CH4和O2的反应为:2CH4(g)+O2(g)![]() 2CO(g)+4H2(g)。设CH4同时和H2O(g)及O2(g)反应。1 m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为____________。
2CO(g)+4H2(g)。设CH4同时和H2O(g)及O2(g)反应。1 m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为____________。
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
气体 | CO | H2 | N2 | O2 |
体积(L) | 25 | 60 | 15 | 2.5 |
计算该富氧空气中O2和N2的体积比V(O2)∶V(N2)。
(4)若CH4和H2O(g)及富氧空气混合反应的产物中,V(H2)∶V(N2)=3∶1(合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为何值?
(6分)合成氨原料可以由天然气制取。
其主要反应为:CH4(g)+H2O(g)→CO(g)+3H2(g)
(1)1m3(标准状况)CH4按上式完全反应,产生H2____________mol。
(计算结果保留整数)
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应。1m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为____________ m3。(填体积取值范围)
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
| 气体 | CO | H2 | N2 | O2 |
| 体积(L) | 25 | 60 | 15 | 2.5 |
计算该富氧空气中O2和N2的体积比V(O2)/V(N2)=