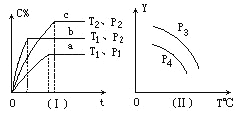题目内容
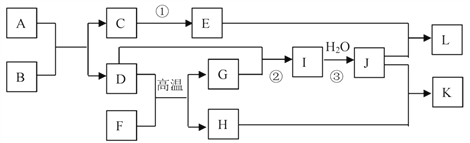
【题目】某化学实验室以一种工业上的废渣(废渣主要含有MgCO3、MgSiO3和少量Fe、Al的氧化物)为原料,制备MgCO3·3H2O。实验流程如下图所示:

(1)为了加快废渣的酸溶速率,可采取的办法有_________(任写一点),酸溶时废渣中主要成分发生反应的离子方程式为___________________________________。
(2)加入30%H2O2的目的是__________________________________。
(3)用萃取分液的方法除去溶液中的Fe3+
①加入30%H2O2后,检验溶液中是否含有Fe2+的最佳试剂是__________________________。
②萃取分液完成后,检验水相中是否含有Fe3+的最佳试剂是______________________________。
(4)室温下,除去MgSO4溶液中的A13+(使Al3+浓度小于1×10-6mol/L)而不引入其它杂质,应加入的试剂X为__________,应调节pH的范围为_________________。
已知:①Ksp[Al(OH)3]=1.0×10-33 ②pH=8.5时,Mg(OH)2开始沉淀
(5)向滤液中加入Na2CO3溶液生成MgCO3沉淀并用蒸馏水洗涤,确认沉淀洗净的操作及现象是____________________________。
(6)下图为不同反应温度下所得水合碳酸镁的X射线衍射谱图。由图可知,干燥时需控制温度范围为___________________,温度较高时MgCO3·3H2O发生转化的化学方程式为_______________________________。

【答案】 升高温度、搅拌、提高硫酸浓度等 MgCO3+2H+=Mg2++H2O+CO2↑ MgSiO3+2H+=Mg2++H2SiO3 将Fe2+氧化为Fe3+ ,便于除去 K3[Fe(CN)6]溶液 KSCN 溶液 MgO、Mg(OH)2、MgCO3或Mg2(OH)2 CO3 5.0 取少量最后一次的洗涤过滤液于试管中,向其中滴加盐酸酸化的氯化钡溶液,若不产生白色沉淀,则表明已洗涤干净 293K~313K(313K以下也可) 5MgCO3·3H2O![]() Mg5(OH)2 (CO3)4·4H2O+CO2↑+10H2O
Mg5(OH)2 (CO3)4·4H2O+CO2↑+10H2O
【解析】(1)为了加快废渣的酸溶速率,可采取的办法有升高温度、搅拌、提高硫酸浓度等,酸溶时废渣中主要成分是碳酸镁和硅酸镁,发生反应的离子方程式为MgCO3+2H+=Mg2++H2O+CO2↑、MgSiO3+2H+=Mg2++H2SiO3。(2)溶液中含有亚铁离子,双氧水具有强氧化性,能把亚铁离子氧化为铁离子,便于除去。(3)①检验溶液中是否含有Fe2+的最佳试剂是K3[Fe(CN)6]溶液。②萃取分液完成后,检验水相中是否含有Fe3+的最佳试剂是KSCN溶液。(4)室温下,除去MgSO4溶液中的A13+(使Al3+浓度小于1×10-6mol/L)而不引入其它杂质,应加入的试剂X为MgO、Mg(OH)2、MgCO3或Mg2(OH)2·CO3。根据氢氧化铝的溶度积常数可知当铝离子浓度是1×10-6mol/L时,氢氧根的浓度是![]() ,又因为pH=8.5时,Mg(OH)2开始沉淀,所以应调节pH的范围为5.0<pH<8.5。(5)沉淀表面含有硫酸根离子,可以通过检验硫酸根离子判断沉淀是否洗涤干净,则确认沉淀洗净的操作及现象是:取少量最后一次的洗涤过滤液于试管中,向其中滴加盐酸酸化的氯化钡溶液,若不产生白色沉淀,则表明已洗涤干净。(6)根据图像可知超过313K时碳酸镁晶体会发生化学变化,所以干燥时需控制温度范围为293K~313K,温度较高时MgCO3·3H2O发生转化生成Mg5(OH)2(CO3)4·4H2O,反应的化学方程式为5MgCO3·3H2O
,又因为pH=8.5时,Mg(OH)2开始沉淀,所以应调节pH的范围为5.0<pH<8.5。(5)沉淀表面含有硫酸根离子,可以通过检验硫酸根离子判断沉淀是否洗涤干净,则确认沉淀洗净的操作及现象是:取少量最后一次的洗涤过滤液于试管中,向其中滴加盐酸酸化的氯化钡溶液,若不产生白色沉淀,则表明已洗涤干净。(6)根据图像可知超过313K时碳酸镁晶体会发生化学变化,所以干燥时需控制温度范围为293K~313K,温度较高时MgCO3·3H2O发生转化生成Mg5(OH)2(CO3)4·4H2O,反应的化学方程式为5MgCO3·3H2O![]() Mg5(OH)2(CO3)4·4H2O+CO2↑+10H2O。
Mg5(OH)2(CO3)4·4H2O+CO2↑+10H2O。