题目内容
【题目】Na2S2O3·5H2O可作为高效脱氯剂,工业上用硫铁矿(FeS2)为原料制备该物质的流程如下。
硫铁矿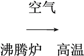
![]()
![]()
![]()
![]()
![]()
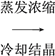 Na2S2O3·5H2O
Na2S2O3·5H2O
已知:Ⅰ.气体A可以使品红溶液褪色,与硫化氢(H2S)混合能获得单质硫。
Ⅱ.pH约为11的条件下,单质硫与亚硫酸盐可以共热生成硫代硫酸盐。
回答下列问题:
(1)沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,其目的是_______________________________。
(2)吸收塔中的原料B可以选用________(填字母序号)。
a.NaCl溶液 b.Na2CO3溶液 c.Na2SO4溶液
(3)某小组同学用下图装置模拟制备Na2S2O3的过程(加热装置已略去)。
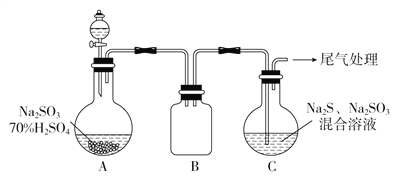
①使用70%的硫酸比用98%的浓硫酸反应速率快,其原因是____________________。装置B的作用是______________________。
②C中制备Na2S2O3发生的连续反应的化学方程式有Na2S+H2O+SO2===Na2SO3+H2S、2H2S+SO2===3S↓+2H2O (或)2H2S+H2SO3===3S↓+3H2O和___________________________________。
(4)工程师设计了从硫铁矿获得单质硫的工艺,将粉碎的硫铁矿用过量的稀盐酸浸取,得到单质硫和硫化氢气体,该反应的化学方程式为__________。
【答案】 使固体与气体充分接触,加快反应速率 b 该反应的实质是H+与SO![]() 反应,70%的硫酸中含水较多,c(H+)和c(SO
反应,70%的硫酸中含水较多,c(H+)和c(SO![]() )都较大,生成SO2速率更快 防止倒吸 Na2SO3+S=Na2S2O3 FeS2+2HCl===FeCl2+H2S↑+S↓
)都较大,生成SO2速率更快 防止倒吸 Na2SO3+S=Na2S2O3 FeS2+2HCl===FeCl2+H2S↑+S↓
【解析】硫铁矿在沸腾炉中燃烧生成氧化铁与二氧化硫,气体A为二氧化硫,溶液D蒸发浓缩、冷却结晶得到硫代硫酸钠晶体,故D为Na2S2O3,单质单质硫与亚硫酸盐可以共热生成硫代硫酸盐,则溶液C为Na2SO3,故原料B为可以为碳酸钠溶液或氢氧化钠溶液。则
(1)沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,其目的是:使固体与气体充分接触,加快反应速率;(2)碳酸钠可以与二氧化硫反应生成亚硫酸钠与二氧化碳,而NaCl、硫酸钠不与二氧化硫反应,答案选b;(3)A为制备二氧化硫,二氧化硫在C中与硫化钠溶液反应得到硫化氢,硫化氢与二氧化硫反应得到S单质,S单质与亚硫酸钠反应得到硫代硫酸钠,C中反应导致装置内压强减小,因此B装置作用是防止倒吸。则
①该反应的实质是H+与SO32-反应,70%的硫酸中含水较多,c(H+)和c(SO32-)都较大,生成SO2速率更快;根据以上分析可知B装置作用是防止倒吸;②C中制备Na2S2O3发生的连续反应有:Na2S+H2O+SO2=Na2SO3+H2S、2H2S+SO2=3S↓+2H2O 或 2H2S+H2SO3=3S↓+3H2O 和Na2SO3+S![]() Na2S2O3;(4)由题目信息可知,FeS2与HCl反应生成H2S、S,同时还生成FeCl2,反应方程式为:FeS2+2HCl===FeCl2+H2S↑+S↓。
Na2S2O3;(4)由题目信息可知,FeS2与HCl反应生成H2S、S,同时还生成FeCl2,反应方程式为:FeS2+2HCl===FeCl2+H2S↑+S↓。
