题目内容
【题目】在2L密闭容器内,800℃时反应:![]() 体系中,n(NO)随时间的变化如下表:
体系中,n(NO)随时间的变化如下表:
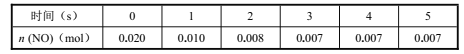
[转化率=(某反应物转化的物质的量/该反应物起始的总的物质的量)×100%]
(1)上述反应 (填“是”或“不是”)可逆反应,在第 5s时,NO的转化率为 ;
(2)下图中表示 NO2变化曲线的是 ;用 O2表示 0~2s内该反应的平均速率υ= ;

(3)能说明该反应已达到平衡状态的是 (填字母序号)。
A.υ(NO2)=2υ(O2) B.容器内压强保持不变
C.υ逆(NO)=2υ正(O2) D.容器内密度保持不变
【答案】(14分,每空2分)
(1)是;65% (2)b;0.0015 mol·L-1·s-1 (3)BC
【解析】
试题分析:(1)从数据分析,最后反应体系仍有一氧化氮,说明反应为可逆反应,故填是;在第5秒时,一氧化氮的转化率为(0.020-0.007)/0.020=65%。(2)从数据分析,随着反应的进行,二氧化氮的物质的量在依次增加,且平衡时二氧化氮的物质的量为(0.020-0.007)/2=0.0065mol/L,故选b;2秒内氧气的物质的量改变量为(0.0020-0.008)/2=0.006mol,其平均反应速率为0.006/2/2=0.0015 mol·L-1·s-1 。(3)A、没有说明反应的方向,不能说明反应到平衡,故错误;B、反应前后物质的量不同,所以压强不变化说明反应到平衡,故正确;C、可以说明反应到平衡,故正确;D、反应体系全为气体,体积不变,则气体的密度保持不变,故不能说明反应到平衡,故错误,故选BC。

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目