��Ŀ����
��1�����������У����ʵ���������________����ԭ�Ӹ���������________������������________��
A��3gH2��B�������33��6LCO2��C��1��204��1024��HCl���ӣ�D��49gH2SO4��E��46g�Ҵ�(C2H5OH)��F��4��ʱ10mLˮ
��2����һ�������£�32gA��22gBǡ�÷�Ӧ����C��9gD������ͬ�����£�8gA������B��Ӧ����D��0��125molC����������ʵ����֪C��Ħ������Ϊ ��
��1��C E C ��2��90g/mol
��������
�����������1��Cѡ������ʵ���Ϊ2mol�����ʵ������Eѡ��ԭ�ӵĸ���Ϊ9NA��ԭ�Ӹ�����ࡣC������Ϊ73g ���������2����Ϊ32 gA��22 gBǡ�÷�Ӧ����C��9 gD�����Եõ�C������Ϊ32+22��9=45g ������8gA��Ӧ����C������Ϊ11��25g������M=m/n������Եõ�C��Ħ������Ϊ90g/mol��
���㣺���ʵ����Ļ������㡣

 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д� ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
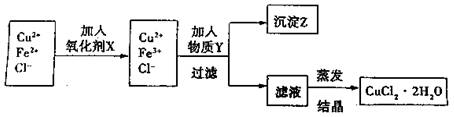
ͬ����չ�Ķ�ϵ�д���15�֣���ȡ�������Ȼ�ͭ���壨CuCl2��2H2O���������������£�
I����������ͭ��������Fe���ܽ���������ϡ�����У�Ȼ����ȡ����˵õ�CuCl2��������FeCl2����Һ�����ⶨ����ҺpHΪ2��
II����I�����õ�����Һ�����в�������ᴿ��
��֪��
|
|
�������↑ʼ����ʱ��pH |
�������������ȫʱ��pH |
|
Fe3+ |
1.9 |
3.2 |
|
Cu2+ |
4.7 |
6.7 |
�Իش��������⣺
��1�����������У����ʺ���Ϊ������X���� ��������ţ�
A��KMnO4 B��K2Cr2O4 C��H2O2 D��NaClO
��2���ټӽ��������Y�� ��
��д������Z��ˮ�еij����ܽ�ƽ�ⷽ��ʽ�� ��
��3�����������Z��������Һ������������Ȼ�ͭ���壨CuCl2��2H2O����Ӧ��ȡ�Ĵ�ʩ�� ��
��4����ijͬѧ���÷�Ӧ��Cu+2H+===Cu2++H2�����ʵ������ȡCuCl2��Һ����ͬѧ��Ƶ�װ��Ӧ��Ϊ �����ԭ��ء����ء���
�����������淽���л�����ͬѧ��Ƶ�װ��ͼ����ָ���缫���Ϻ͵������Һ��

��5����֪һЩ�������Ũ�Ȼ��������±���
|
���� |
FeS |
MnS |
CuS |
PbS |
HgS |
ZnS |
|
Ksp |
6.3��10-18 |
2.5��-13 |
1.3��10-36 |
3.4��10-28 |
6.4��10-53 |
1.6��10-24 |
ij��ҵ��ˮ�к���Cu2+��Pb2+��Hg2+����������˹�ҵ��ˮ�м�������� ��ȥ���ǡ���ѡ����ţ�
��NaOH ��FeS ��Na2S
��15�֣���ȡ�������Ȼ�ͭ���壨CuCl2��2H2O���������������£�
I����������ͭ��������Fe���ܽ���������ϡ�����У�Ȼ����ȡ����˵õ�CuCl2��������FeCl2����Һ�����ⶨ����ҺpHΪ2��
II����I�����õ�����Һ�����в�������ᴿ��

��֪��
|
|
�������↑ʼ����ʱ��pH |
�������������ȫʱ��pH |
|
Fe3+ |
1.9 |
3.2 |
|
Cu2+ |
4.7 |
6.7 |
�Իش��������⣺
��1�����������У����ʺ���Ϊ������X���� ��������ţ�
A��KMnO4 B��K2Cr2O4 C��H2O2 D��NaClO
��2���ټӽ��������Y�� ��
��д������Z��ˮ�еij����ܽ�ƽ�ⷽ��ʽ�� ��
��3�����������Z��������Һ������������Ȼ�ͭ���壨CuCl2��2H2O����Ӧ��ȡ�Ĵ�ʩ�� ��
��4����ijͬѧ���÷�Ӧ��Cu+2H+===Cu2++H2�����ʵ������ȡCuCl2��Һ����ͬѧ��Ƶ�װ��Ӧ��Ϊ �����ԭ��ء����ء���
�����������淽���л�����ͬѧ��Ƶ�װ��ͼ����ָ���缫���Ϻ͵������Һ��

��5����֪һЩ�������Ũ�Ȼ��������±���
|
���� |
FeS |
MnS |
CuS |
PbS |
HgS |
ZnS |
|
Ksp |
6.3��10-18 |
2.5��-13 |
1.3��10-36 |
3.4��10-28 |
6.4��10-53 |
1.6��10-24 |
ij��ҵ��ˮ�к���Cu2+��Pb2+��Hg2+����������˹�ҵ��ˮ�м�������� ��ȥ���ǡ���ѡ����ţ�
��NaOH ��FeS ��Na2S


 Fe2+��aq��+3OH-��aq��
Fe2+��aq��+3OH-��aq�� ˮ��������ԴȪ��Ҳ�Dz���ȱ�ٵ���Դ��
ˮ��������ԴȪ��Ҳ�Dz���ȱ�ٵ���Դ��