题目内容
 某同学采用如图装置进行实验,证明了铜与稀硝酸反应生成了NO.实验时,先向注射器内加入一定量的稀硝酸,排净注射器内的空气,迅速将带有铜丝的橡皮帽盖上,一段时间后,注射器内有无色气体产生.
某同学采用如图装置进行实验,证明了铜与稀硝酸反应生成了NO.实验时,先向注射器内加入一定量的稀硝酸,排净注射器内的空气,迅速将带有铜丝的橡皮帽盖上,一段时间后,注射器内有无色气体产生.(1)请写出铜与稀硝酸反应的化学方程式
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
.(2)若证明无色气体是NO的实验操作和现象是
取下橡皮帽,无色气体变为红棕色(或注射器出口处有红棕色气体)
取下橡皮帽,无色气体变为红棕色(或注射器出口处有红棕色气体)
.一氧化氮是大气污染物之一.目前,有一种治理方法是在400℃左右、有催化剂存在的情况下,用氨把一氧化氮还原为氮气和水.该反应的化学方程式为4NH3+6NO═5N2+6H2O 每有10mol N2生成,被还原的氧化剂为
12
12
mol.(3)若将上述稀硝酸换成浓硝酸,其生成的气体为
NO2
NO2
,将此气体通入水中,发生反应的化学方程式为3NO2+H2O═2HNO3+NO
3NO2+H2O═2HNO3+NO
.分析:(1)铜和稀硝酸反应生成NO气体;
(2)根据NO与氧气反应生成红棕色NO2的性质检验;反应4NH3+6NO═5N2+6H2O中,NO为氧化剂,NH3为还原剂,每生成5molN2,有6molNO被还原;
(3)铜和浓硝酸反应生成NO2,NO2可与水反应生成硝酸和NO.
(2)根据NO与氧气反应生成红棕色NO2的性质检验;反应4NH3+6NO═5N2+6H2O中,NO为氧化剂,NH3为还原剂,每生成5molN2,有6molNO被还原;
(3)铜和浓硝酸反应生成NO2,NO2可与水反应生成硝酸和NO.
解答:解:(1)铜和稀硝酸反应生成NO气体,反应的化学方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,故答案为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;
(2)NO与氧气反应生成红棕色NO2,可取下橡皮帽,无色气体变为红棕色(或注射器出口处有红棕色气体),说明无色气体为NO,反应4NH3+6NO═5N2+6H2O中,NO为氧化剂,NH3为还原剂,每生成5molN2,有6molNO被还原,则每有10molN2生成,被还原的氧化剂为12mol,
故答案为:取下橡皮帽,无色气体变为红棕色(或注射器出口处有红棕色气体);12;
(3)铜和浓硝酸反应生成NO2,NO2可与水反应生成硝酸和NO,反应的方程式为3NO2+H2O═2HNO3+NO,故答案为:NO2;3NO2+H2O═2HNO3+NO.
(2)NO与氧气反应生成红棕色NO2,可取下橡皮帽,无色气体变为红棕色(或注射器出口处有红棕色气体),说明无色气体为NO,反应4NH3+6NO═5N2+6H2O中,NO为氧化剂,NH3为还原剂,每生成5molN2,有6molNO被还原,则每有10molN2生成,被还原的氧化剂为12mol,
故答案为:取下橡皮帽,无色气体变为红棕色(或注射器出口处有红棕色气体);12;
(3)铜和浓硝酸反应生成NO2,NO2可与水反应生成硝酸和NO,反应的方程式为3NO2+H2O═2HNO3+NO,故答案为:NO2;3NO2+H2O═2HNO3+NO.
点评:本题考查无机化合物知识,侧重于硝酸、氮氧化物的性质的考查,解答该类题目,检验加强基础知识的学习,掌握物质的性质、反应现象以及有关反应方程式的书写,题目难度不大.

练习册系列答案
相关题目
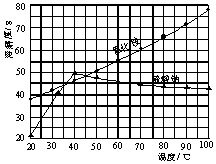
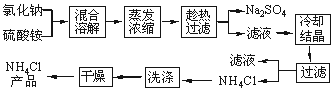
 (3)实验过程中趁热过滤的目的是 。趁热过滤可采用抽滤装置,抽滤装置如图1所示,该装置中的错误之处是 ;若用普通的漏斗,贴上滤纸后,接上抽滤瓶进行吸滤则不行,因为 。
(3)实验过程中趁热过滤的目的是 。趁热过滤可采用抽滤装置,抽滤装置如图1所示,该装置中的错误之处是 ;若用普通的漏斗,贴上滤纸后,接上抽滤瓶进行吸滤则不行,因为 。