题目内容
反应mA(g)+nB(g)压强/Pa | 2×105 | 5×105 | 1×106 |
c(A)/mol·L-1 | 0.08 | 0.20 | 0.44 |
分析表中数据,完成:?
(1)当压强从2×105 Pa增加到5×105 Pa时,平衡_______(填“向左”“向右”或“不”)移动,理由是_____________________。?
(2)当压强从5×105 Pa增加到1×106 Pa时,该反应的化学平衡_______移动,判断的依据是____________________________,可能的原因是____________________________。
解析:本题考查的是化学平衡状态的比较,这是近年出现的新题型。提取出解题有关信息,考查了数学应用能力;选材上,同一反应在一定压强段,化学平衡不受压强影响,而在另一压强段却受压强影响,具有迷惑性,我们要能打破“物质的状态一定”的思维定势,具有创新思维能力。①由压强比与浓度比的比较,判断平衡移动方向;②突破常规思维,想到B的状态可变。(1)![]() =2.5,说明浓度的变化只与体积变化有关,化学反应对它无影响,即化学平衡不移动。(2)
=2.5,说明浓度的变化只与体积变化有关,化学反应对它无影响,即化学平衡不移动。(2)![]() =2.2,说明p改变,化学平衡向生成A的方向移动了,由(1)知n+m=x,故必然是升压时,B液化造成逆反应为气体分子数减少的方向。?
=2.2,说明p改变,化学平衡向生成A的方向移动了,由(1)知n+m=x,故必然是升压时,B液化造成逆反应为气体分子数减少的方向。?
答案:(1)不 当p增大2.5倍时,c(A)增大2.5倍,说明平衡没有移动,即m+n=x?
(2)向左 当p增大2倍时,c(A)却增大了2.2倍,说明平衡向生成A的方向移动 增大压强时,B转化为液态?

练习册系列答案
相关题目
 pC(g)+ qD(g)在一密闭容器中进行,测得平均反应速度v(C)= 2v(B)。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是 ( )
pC(g)+ qD(g)在一密闭容器中进行,测得平均反应速度v(C)= 2v(B)。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是 ( ) cC(g)+dD(g),C物质的质量分数w(C)与温度、压强的关系如图所示,下列判断正确的是(
)
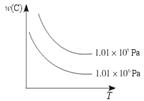
cC(g)+dD(g),C物质的质量分数w(C)与温度、压强的关系如图所示,下列判断正确的是(
)
 cC(g)+dD(g),C物质的体积分数(C%)与温度、压强的关系如图所示,下列判断正确的是( )
cC(g)+dD(g),C物质的体积分数(C%)与温度、压强的关系如图所示,下列判断正确的是( )