题目内容
【题目】[化学一物质结构与性质]
硒化锌是一种半导体材料,回答下列问题。
(1)锌在周期表中的位置_____________;Se基态原子价电子排布图为___________。元素锌、硫和硒第一电离能较大的是______________________(填元素符号)。
(2)Na2SeO3分子中Se原子的杂化类型为___________;H2SeO4的酸性比H2SeO3强,原因是_________________________________________________。
(3)气态SeO3分子的立体构型为__________;下列与SeO3互为等电子体的有____(填序号)。
A.CO32- B.NO3- C.NCl3 D.SO32-
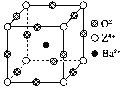
(4)硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为_____(填元素符号);该晶胞中硒原子所处空隙类型为______________(填“立方体”、“正四面体”或正八面体”),该种空隙的填充率为____________;若该晶胞密度为pg·cm-3,硒化锌的摩尔质量为Mg·mol-1。用NA代表阿伏加德罗常数的数值,则晶胞参数a为_____nm。

【答案】 第四周期IIB族 ![]() S sp3 H2SeO4的非羟基氧比H2SeO3多(或H2SeO4中Se的化合价更高) 平面三角形 AB Zn 正四面体 50%
S sp3 H2SeO4的非羟基氧比H2SeO3多(或H2SeO4中Se的化合价更高) 平面三角形 AB Zn 正四面体 50%  ×107
×107
【解析】(1) Zn的原子序数是30,其电子排布式为1s22s22p63s23p63d104s2,由电子排布式可知该元素为第四周期ⅡB族;Se的原子核外有34个电子,最外层有6个电子,则其核外电子分4层排布,最外层为电子排布为4s24p4,基态原子价电子排布图为![]() ;锌金属性较强,第一电离能较小,S的非金属性强于As,第一电离能最大,即元素锌、硫和硒第一电离能较大的是S;(2)Na2SeO3分子中Se原子的价层电子对数为
;锌金属性较强,第一电离能较小,S的非金属性强于As,第一电离能最大,即元素锌、硫和硒第一电离能较大的是S;(2)Na2SeO3分子中Se原子的价层电子对数为![]() =4,所以Se杂化方式为sp3杂化;H2SeO4的非羟基氧比H2SeO3多(或H2SeO4中Se的化合价更高),故H2SeO4的酸性比H2SeO3强;(3)SeO3的价层电子对数是3,Se原子上无孤电子对,故分子的立体构型是平面三角形;等电子体要求原子总数相同,价电子数相同,所以与SeO3互为等电子体的一种离子为CO32-或NO3-等,答案选AB;(4)硒化锌的晶胞结构中原子个数比为1:1,其中Se原子4个,若X和Y点所堆积的原子均为Zn原子,则
=4,所以Se杂化方式为sp3杂化;H2SeO4的非羟基氧比H2SeO3多(或H2SeO4中Se的化合价更高),故H2SeO4的酸性比H2SeO3强;(3)SeO3的价层电子对数是3,Se原子上无孤电子对,故分子的立体构型是平面三角形;等电子体要求原子总数相同,价电子数相同,所以与SeO3互为等电子体的一种离子为CO32-或NO3-等,答案选AB;(4)硒化锌的晶胞结构中原子个数比为1:1,其中Se原子4个,若X和Y点所堆积的原子均为Zn原子,则![]() ,符合;则图中X和Y点所堆积的原子均为Zn原子;根据图中原子位置可知,该晶胞中硒原子所处空隙类型为正四面体,该种空隙的填充率为50%;若该晶胞密度为pg·cm-3,硒化锌的摩尔质量为Mg·mol-1。用NA代表阿伏加德罗常数的数值,根据
,符合;则图中X和Y点所堆积的原子均为Zn原子;根据图中原子位置可知,该晶胞中硒原子所处空隙类型为正四面体,该种空隙的填充率为50%;若该晶胞密度为pg·cm-3,硒化锌的摩尔质量为Mg·mol-1。用NA代表阿伏加德罗常数的数值,根据 ,所以V=
,所以V=![]() ,则晶胞的边长为
,则晶胞的边长为 cm=
cm= ×107 nm。
×107 nm。