题目内容
将1.92克铜粉与一定量的浓硝酸反应,当铜粉完全作用时,用排水法收集的气体在标况下的体积可能为 ( )
A.1.12L B.0.56L C.0.448L D.0.224L
【答案】
C
【解析】
试题分析:1.92g铜的物质的量是1.92g÷64g/mol=0.03mol,则根据电子的得失守恒可知,生成的NO2的物质的量是0.06mol。又因为NO2溶于水生成NO,所以根据反应的方程式3NO2+H2O=2HNO3+NO可知, NO的体积是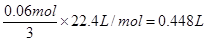 ,答案选C。
,答案选C。
考点:考查浓硝酸和铜反应的有关计算
点评:该题是基础性试题的考查,难度不大,属于常规性计算题的考查,难度不大。学生只要能熟练掌握有关反应的化学方程式,然后直接列式计算即可。

练习册系列答案
相关题目