题目内容
将6 mol H2和3 mol CO充入容积为0.5 L的密闭容器中,进行如下反应:
2 H2(g) + CO(g) CH3OH(g),6秒时体系达到平衡,此时容器内压强为开始时的0.6倍,
CH3OH(g),6秒时体系达到平衡,此时容器内压强为开始时的0.6倍,
求:(1)H2的反应速率;(2)CO的转化率。
2 H2(g) + CO(g)
 CH3OH(g),6秒时体系达到平衡,此时容器内压强为开始时的0.6倍,
CH3OH(g),6秒时体系达到平衡,此时容器内压强为开始时的0.6倍,求:(1)H2的反应速率;(2)CO的转化率。
(1)1.2 mol·(L·s)—1 (2)60%
试题分析: 2 H2(g) + CO(g)
 CH3OH(g)
CH3OH(g)起始浓度(mol/L) 12 6 0
转化浓度(mol/L) 2x x x
平衡浓度(mol/L) 12-2x 6-x x
则
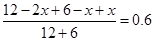
解得x=3.6mol/L
则H2的反应速率是
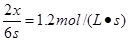
CO的转化率是
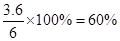
点评:该题是高考中的常见考点,属于基础性试题的考查,难度不大。主要是考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的规范答题能力和应试能力。该类试题需要注意的是在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案
相关题目
 A(g)+2B(g),已知ΔH<0,下列判断正确的是
A(g)+2B(g),已知ΔH<0,下列判断正确的是 2NH3(g) △H<0,其他条件不变时,升高温度,反应速率v(H2)和H2的平衡转化率α(H2)均增大
2NH3(g) △H<0,其他条件不变时,升高温度,反应速率v(H2)和H2的平衡转化率α(H2)均增大 H2(g)+I2(g紫色),下列叙述能够说明已达平衡状态的是( )
H2(g)+I2(g紫色),下列叙述能够说明已达平衡状态的是( )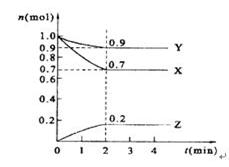
 CO2(g) + H2(g) △H <0
CO2(g) + H2(g) △H <0