题目内容
【题目】下列关于Fe(OH)3胶体的叙述中,正确的是( )
A. 制备Fe(OH)3胶体的化学方程式是FeCl3+3H2O![]() Fe(OH)3↓+3HCl
Fe(OH)3↓+3HCl
B. 在制备Fe(OH)3胶体的实验中,加热煮沸时间越长,越有利于胶体的生成
C. Fe(OH)3胶体微粒能吸附阳离子,从而使Fe(OH)3胶体带有一定电荷
D. Fe(OH)3胶体能够吸附水中悬浮的固体颗粒并沉降,达到净水目的
【答案】D
【解析】
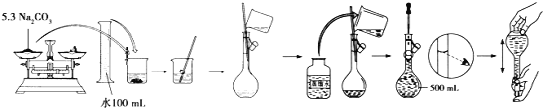
A项、将饱和的氯化铁溶液滴入到沸水中,并继续煮沸至溶液呈红褐色,停止加热制得氢氧化铁胶体,反应的化学方程式为FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl,故A错误;
Fe(OH)3(胶体)+3HCl,故A错误;
B项、制备氢氧化铁胶体时,当溶液变成红褐色时,停止加热,不能在长时间加热得原因是胶体会受热聚沉,故B错误;
C项、氢氧化铁胶体不带电,氢氧化铁胶体粒子具有较大的表面积,具有吸附性,能吸附阳离子带正电荷,故C错误;
D项、氢氧化铁胶体粒子具有较大的表面积,具有吸附性,能够吸附水中悬浮的固体颗粒并沉降,达到净水目的,故D正确;
故选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某工业流程中,进入反应塔的混合气体中NO和O2的物质的量分数分別为0.10和0.06,发生化学反应2NO(g)+O2(g) ![]() 2NO2(g),在其他条件相同时,测得实验数据如下表:
2NO2(g),在其他条件相同时,测得实验数据如下表:
压强/(×105Pa) | 温度/℃ | NO达到所列转化率需要时间/s | ||
50% | 90% | 98% | ||
1.0 | 30 | 12 | 250 | 2830 |
90 | 25 | 510 | 5760 | |
8.0 | 30 | 0.2 | 3.9 | 36 |
90 | 0.6 | 7.9 | 74 | |
根据表中数据,下列说法正确的是
A.升高温度,反应速率加快
B.增大压强,反应速率变慢
C.在1.0×105 Pa、90℃条件下,当转化率为98%时反应已达平衡
D.若进入反应塔的混合气体为a mol,反应速率以![]() 表示,则在8.0×105Pa、30℃条件下,转化率从50%增至90%时段NO的反应速率为
表示,则在8.0×105Pa、30℃条件下,转化率从50%增至90%时段NO的反应速率为![]() mols-1
mols-1