题目内容
【题目】现有两份氨水。一份质量分数为 w%,物质的量浓度为c1 mol· L-1;另一份质量分数为2w%,物质的量浓度为c2 mol· L-1。下列说法不正确的是
A.c2<2c1
B.将两溶液等体积混合后,所得溶液的物质的量浓度为0.5(c1+c2)mol· L-1
C.将两溶液等质量混合后,取100mL 混合溶液,可恰好与 0.05(c1+c2)molCuSO4反应使Cu2+完全沉淀
D.向 100g 质量分数为 2w%的氨水中加入 100g水,即得质量分数为 w%的氨水
【答案】C
【解析】
试题分析:A.根据c= ![]() 可得,
可得,![]() =
= 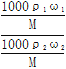 =
= ![]() =
= ![]() ,因氨水的质量分数越大,密度越小,则有ρ1>ρ2,即:
,因氨水的质量分数越大,密度越小,则有ρ1>ρ2,即:![]() >
>![]() ,即:c2<2c1,故A正确;B.将两溶液等体积混合后,所得混合溶液溶质的物质的量不变,根据稀释公式可得,c混V混=c1V1+c2V2,即:c混×2V=c1V+c2V,则所得溶液的物质的量浓度为0.5(c1+c2)mol·L-1,故B正确;C.0.05(c1+c2)mol CuSO4恰好完全沉淀需0.1(c1+c2)mol 氨水,将两溶液等质量混合后,混合液的质量分数为1.5w%,混合液的物质的量浓度小于(c1+c2)mol·L-1,故C错误;D.根据稀释公式m混w混=m1w1+m2w2可得,根据向 100g 质量分数为 2w%的氨水中加入 100g水,即得质量分数为 w%的氨水,故D正确。故选C。
,即:c2<2c1,故A正确;B.将两溶液等体积混合后,所得混合溶液溶质的物质的量不变,根据稀释公式可得,c混V混=c1V1+c2V2,即:c混×2V=c1V+c2V,则所得溶液的物质的量浓度为0.5(c1+c2)mol·L-1,故B正确;C.0.05(c1+c2)mol CuSO4恰好完全沉淀需0.1(c1+c2)mol 氨水,将两溶液等质量混合后,混合液的质量分数为1.5w%,混合液的物质的量浓度小于(c1+c2)mol·L-1,故C错误;D.根据稀释公式m混w混=m1w1+m2w2可得,根据向 100g 质量分数为 2w%的氨水中加入 100g水,即得质量分数为 w%的氨水,故D正确。故选C。

练习册系列答案
相关题目