��Ŀ����
18��G��һ�ֺϳ�����֬����Ҫԭ�ϣ�A��C��H��O����Ԫ����ɵ���Ԫ��״�������Է�������Ϊ98��������Ԫ�ص���������Ϊ49%����˴Ź�������ֻ��һ���壻F�ĺ˴Ź���������3���壬�����֮��Ϊ2��2��3����֪��������R����������
 ��RCOOH$\stackrel{LiAlH_{4}}{��}$RCH2OH
��RCOOH$\stackrel{LiAlH_{4}}{��}$RCH2OH�й����ʵ�ת����ϵ��ͼ��ʾ����ش��������⣮
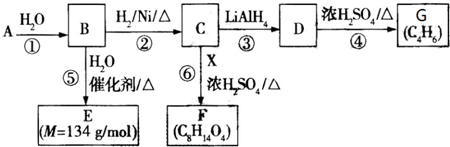
��1��B�к��������ŵ��������Ȼ���A�Ľṹ��ʽΪ
 ��
���ݵķ�Ӧ�����Ǽӳɷ�Ӧ��G��Br2��CCl4��Һ��Ӧ�����п��ܵIJ��ﹲ��3�֣�
��2����Ӧ�ܵĻ�ѧ����ʽΪ
 ��
����3��E����һ�����������ɸ߷��ӻ����д���ø߷��ӻ�������ܵĽṹ��ʽ��
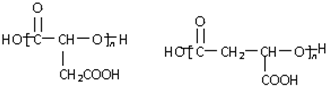 ��
����4����Ӧ�Ļ�ѧ����ʽΪHOOCCH2CH2COOH+2C2H5OH
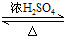 CH3CH2OOCCH2CH2COOCH2CH3+2H2O��
CH3CH2OOCCH2CH2COOCH2CH3+2H2O����5���л���Y��E��Ϊͬ���칹�壬�Ҿ�����ͬ�Ĺ������������Ŀ��д�����з���������Y�Ľṹ��ʽ
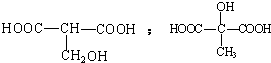 ��
��
���� A��һ����Ԫ��״�������˴Ź�������ֻ��һ���壬˵��A��ֻ��һ�����͵�Hԭ�ӣ�A��ˮ������B��B�ܺ����������ӳɷ�Ӧ����C����������Ϣ��A�ķ���ʽ֪��A�л�����̼̼˫������A�Ľṹ��ʽΪ�� ����BΪHOOCCH=CHCOOH��CΪHOOCCH2CH2COOH��C������Ϣ�еķ�Ӧ�õ�DΪHOCH2CH2CH2CH2OH����G�ķ���ʽ��֪��D������ȥ��Ӧ����G����GΪCH2=CHCH=CH2��B��ˮ������Ӧ����E������B��E��Ħ������֪��B��ˮ�����ӳɷ�Ӧ����E������EΪHOOCCH2CH��OH��COOH��C��X��Ӧ����F������F�ķ���ʽ֪��X���Ҵ���F�Ľṹ��ʽΪCH3CH2OOCCH2CH2COOCH2CH3���ݴ˽��
����BΪHOOCCH=CHCOOH��CΪHOOCCH2CH2COOH��C������Ϣ�еķ�Ӧ�õ�DΪHOCH2CH2CH2CH2OH����G�ķ���ʽ��֪��D������ȥ��Ӧ����G����GΪCH2=CHCH=CH2��B��ˮ������Ӧ����E������B��E��Ħ������֪��B��ˮ�����ӳɷ�Ӧ����E������EΪHOOCCH2CH��OH��COOH��C��X��Ӧ����F������F�ķ���ʽ֪��X���Ҵ���F�Ľṹ��ʽΪCH3CH2OOCCH2CH2COOCH2CH3���ݴ˽��
��� �⣺A��һ����Ԫ��״�������˴Ź�������ֻ��һ���壬˵��A��ֻ��һ�����͵�Hԭ�ӣ�A��ˮ������B��B�ܺ����������ӳɷ�Ӧ����C����������Ϣ��A�ķ���ʽ֪��A�л�����̼̼˫������A�Ľṹ��ʽΪ�� ����BΪHOOCCH=CHCOOH��CΪHOOCCH2CH2COOH��C������Ϣ�еķ�Ӧ�õ�DΪHOCH2CH2CH2CH2OH����G�ķ���ʽ��֪��D������ȥ��Ӧ����G����GΪCH2=CHCH=CH2��B��ˮ������Ӧ����E������B��E��Ħ������֪��B��ˮ�����ӳɷ�Ӧ����E������EΪHOOCCH2CH��OH��COOH��C��X��Ӧ����F������F�ķ���ʽ֪��X���Ҵ���F�Ľṹ��ʽΪCH3CH2OOCCH2CH2COOCH2CH3��
����BΪHOOCCH=CHCOOH��CΪHOOCCH2CH2COOH��C������Ϣ�еķ�Ӧ�õ�DΪHOCH2CH2CH2CH2OH����G�ķ���ʽ��֪��D������ȥ��Ӧ����G����GΪCH2=CHCH=CH2��B��ˮ������Ӧ����E������B��E��Ħ������֪��B��ˮ�����ӳɷ�Ӧ����E������EΪHOOCCH2CH��OH��COOH��C��X��Ӧ����F������F�ķ���ʽ֪��X���Ҵ���F�Ľṹ��ʽΪCH3CH2OOCCH2CH2COOCH2CH3��
��1��BΪHOOCCH=CHCOOH�����к��������ŵ������ǣ��Ȼ���A�Ľṹ��ʽΪ ����Ӧ����HOOCCH=CHCOOH��ˮ�����ӳɷ�Ӧ����HOOCCH2CH��OH��COOH��GΪCH2=CHCH=CH2����Br2��CCl4��Һ��Ӧ��������ȫ�ӳɣ����Է���1��2-�ӳɣ�Ҳ���Է���1��4-�ӳɣ���Ӧ������3�֣�
����Ӧ����HOOCCH=CHCOOH��ˮ�����ӳɷ�Ӧ����HOOCCH2CH��OH��COOH��GΪCH2=CHCH=CH2����Br2��CCl4��Һ��Ӧ��������ȫ�ӳɣ����Է���1��2-�ӳɣ�Ҳ���Է���1��4-�ӳɣ���Ӧ������3�֣�
�ʴ�Ϊ���Ȼ��� ���ӳɷ�Ӧ��3��
���ӳɷ�Ӧ��3��
��2����Ӧ�ܵĻ�ѧ����ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��3����E[HOOCCH2CH��OH��COOH]��һ�������·������۷�Ӧ���ɸ߾���߾���Ľṹ��ʽΪ��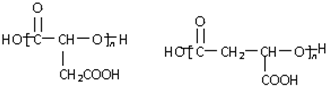 ��
��
�ʴ�Ϊ��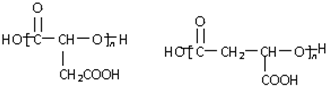 ��
��
��4����Ӧ�Ļ�ѧ����ʽΪ��HOOCCH2CH2COOH+2C2H5OH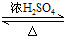 CH3CH2OOCCH2CH2COOCH2CH3+2H2O��
CH3CH2OOCCH2CH2COOCH2CH3+2H2O��
�ʴ�Ϊ��HOOCCH2CH2COOH+2C2H5OH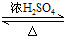 CH3CH2OOCCH2CH2COOCH2CH3+2H2O��
CH3CH2OOCCH2CH2COOCH2CH3+2H2O��
��5���л���Y��E[HOOCCH2CH��OH��COOH]��Ϊͬ���칹�壬�ҹ����ŵ��������Ŀ��ͬ�����з���������H�Ľṹ��ʽ�У�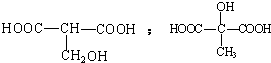 ��
��
�ʴ�Ϊ��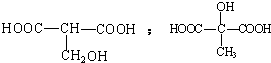 ��
��
���� ���⿼���л����ƶϡ��л���Ӧ���͡������š�ͬ���칹��ȣ��ؼ����ƶ�A�Ľṹ��ע�������л������ʽ�뷴Ӧ���������ƶϣ���ȷ�л���Ķϼ��ͳɼ���ʽ�ǽ���л���Ĺؼ�����Ҫѧ���Ը������Ϣ�������ã��Ѷ��еȣ�

 ��У����ϵ�д�
��У����ϵ�д�| A�� |  | B�� |  | C�� |  | D�� |  |
��֤��Ư�۾��к���CaCl2
����Ư�۾������еμ�����Ũ���ᣬ�۲쵽����ɫ�������ɣ�д�����ɻ���ɫ����Ļ�ѧ��Ӧ����ʽ��Ca��ClO��2+CaCl2+4H2SO4��Ũ��=2Ca��HSO4��2+2Cl2��+2H2O
����Ca��ClO��2+CaCl2+2H2SO4��Ũ��=CaSO4+2Cl2��+2H2O����
�ڽ����ɵĻ���ɫ���建��ͨ��������ʯ�ң���ʯ�����أ����ռ�����ɫ���壮�Ʋ����������г�Cl2��������HCl��O2���ѧʽ����
��֤��Ư�۾��к���Ca��OH��2[��֪���볣����Ka1��H2CO3����Ka��HClO����Ka2��H2CO3��]
�ٽ�����Ư�۾�����ˮ�ⶨ��pHֵΪ12.3�����õIJⶨ����������c��ѡ��𰸱�ţ���
a��ʹ�ù㷺pH��ֽ b��ʹ�þ���pH��ֽc��ʹ��pH�� d���Է�̪Ϊָʾ����������к͵ζ�
������̽�����������У���֤���ý������������a��ѡ��𰸱�ţ���
a����Ư�۾���Һ��ͨ������CO2���ⶨ��Һ��pHֵ�仯
b����Ư�۾���Һ�м�������̼�����ƹ��壬�ⶨ��ҺpHֵ�仯
c����Ư�۾���Һ�м��������������ƹ��壬�ⶨ��ҺpHֵ�仯 ��
�ⶨƯ�۾�����Ч�ɷֵĺ���
��ʵ��ԭ����ClO-+2I-+2H+=Cl-+I2+H2O�� I2+2S2O32-=2I-+S4O62-
��ʵ�鲽�衿
i����ȡ7.740gƯ�۾����壬�ܽ⣬���250mL��Һ��
ii����ȡ����Һ5.00mL����ƿ���������KI��Һ���ữ��������ָʾ����
iii����0.100mol/L Na2S2O3����Һ�ζ����յ㣬��¼ʼĩ������
iv���ظ�ii��iii��������¼ʼĩ������
�ٸ�ʵ����Ҫʹ�õĶ���������������ƽ��еζ��ܡ�250mL����ƿ��д���ƣ���
�ڲ���ii�м����ָʾ��Ϊ���ۣ�д���ƣ������۲쵽��Һ����ɫ��Ϊ��ɫ���Ұ�����ڲ��仯
ʱ���ﵽ�ζ��յ㣮
��ʵ���������£�
| ʵ���� | 1 | 2 | 3 |
| ����Na2S2O3���/mL | 26.90 | 27.00 | 26.95 |
�ܸ�Ư�۾���Ca��ClO��2����������Ϊ��������ֵ�ƣ�0.624������3λ��Ч���֣���
�����һ����Һ�м���AgNO3��Һ���г���������
����ڶ�����Һ�м�������NaOH��Һ����ȣ��ռ�������0.04mol��
�����������Һ�м�������BaCl2��Һ���õ�����6.27g������������ϴ�Ӻ�ʣ���������Ϊ2.33g����������ʵ���У������Ʋ���ȷ���ǣ�������
| A�� | K+һ�����ڣ���c��K+����0.2mol•L-1 | B�� | 100mL��Һ�к�CO32-0.01mol | ||
| C�� | K+��һ������ | D�� | Cl-һ������ |
| A�� | ���ӣ�C6H5OH���ܸ�NaOH��Һ��Ӧ���Ҵ����� | |
| B�� | ��ϩ�ܷ����ӳɷ�Ӧ�����鲻�� | |
| C�� | �ױ���ʹKMnO4������Һ��ɫ�����鲻�� | |
| D�� | ����50�桫60��ʱ����������Ӧ���ױ���30��ʱ���� |
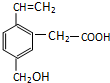 ij�л���Ľṹ��ͼ��ʾ�������л��ﲻ���ܾ��е������ǣ�������
ij�л���Ľṹ��ͼ��ʾ�������л��ﲻ���ܾ��е������ǣ��������ٿ��������������ӳɷ�Ӧ������ʹ����KMnO4��Һ��ɫ��
���ܸ�NaOH��Һ��Ӧ�� ���ܷ���������Ӧ��
���ܷ����Ӿ۷�Ӧ�����ܷ���ˮ�ⷴӦ��
| A�� | �٢� | B�� | ֻ�Т� | C�� | ֻ�Т� | D�� | �ܢ� |
| A�� | ���������� | B�� | ����̼��� | ||
| C�� | ����Ȼ�����Һ | D�� | �Ȼ�þ�����۸��¹��� |
| A�� | ���� | B�� | ���� | C�� | ��ϩ | D�� | �� |
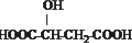
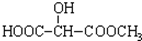 B��
B�� C��H3COOC-COOCH3
C��H3COOC-COOCH3 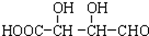 E��
E��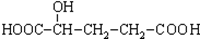
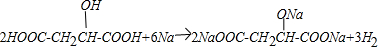 ��
��