题目内容
【题目】铁、钴、镍的性质非常相似,它们的化合物应用十分广泛。回答下列问题:
(1)基态铁原子的价电子排布式为_______。铁、钴、镍的基态原子核外未成对电子数最多的是________。
(2)CoCl2溶于氨水并通入空气,可从溶液中结晶出橙黄色的[Co(NH3)6]Cl3晶体。该配合物中配体分子的立体构型是_______,其中心原子的杂化轨道类型为_________。
(3)铁、镍易与CO作用形成羰基配合物Fe(CO)5、Ni(CO)4,Fe(CO)5的熔点为253K, 沸点为376K,则Ni(CO)4固体属于_____晶体,其中存在的化学键类型为_________。
(4)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO_______FeO (填 “>”“<” 或“=”),原因是___________。
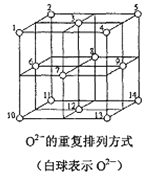
(5)Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的O2-围成的正四面体空隙和3、6、7、8、9、12的O2-围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,正四面体空隙数与O2-数之比为______,有_____%的正八面体空隙没有填充阳离子。Fe3O4晶胞中有8个图示结构单元,晶体密度为5.18g/cm3,则该晶胞参数a=_____pm。(写出计算表达式)
【答案】 3d64s2 铁(或Fe) 三角锥形 sp3 分子 配位键、共价键 > 相同电荷的离子,半径越小,离子间的静电作用力越大,离子晶体的晶格能越大 2∶1 50% ![]() ×1010
×1010
【解析】(1)铁是26号元素,基态铁原子的价电子排布式为3d64s2。钴、镍的基态原子的价电子排布式分别为3d74s2、3d84s2,三种元素原子的核外未成对电子数分别为4、3、2,未成对电子数最多的是铁,故答案为:3d64s2;铁;
(2)在[Co(NH3)6]Cl3晶体中配体分子是氨气分子,氨气分子中N原子的价层电子对个数=3+ ![]() (5-3×1)=3+1=4,立体构型是三角锥形,其中心原子的杂化轨道类型为sp3,故答案为:三角锥形;p3;
(5-3×1)=3+1=4,立体构型是三角锥形,其中心原子的杂化轨道类型为sp3,故答案为:三角锥形;p3;
(3)Fe(CO)5的熔点为253K,沸点为376K,熔沸点较低,因此Ni(CO)4的熔沸点也较低,Ni(CO)4固体属于分子晶体,存在的化学键有配位键、共价键,故答案为:分子;配位键、共价键;
(4)NiO、FeO的晶体结构类型均与氯化钠的相同,说明二者都是离子晶体,离子晶体的熔点与离子键的强弱有关,离子所带电荷数越多,离子半径越小,离子键越强,熔点越高.由于Ni2+的离子半径小于Fe2+的离子半径,所以熔点是NiO>FeO,故答案为:>;相同电荷的离子,半径越小,离子间的静电作用力越大,离子晶体的晶格能越大;
(5)结构中如1、3、6、7的O2-围成的正四面体空隙有8个,由图可知晶体结构中O2-离子数目为8×![]() +6×
+6×![]() =4,故正四面体空隙数与O2-离子数目之比8:4=2:1;Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,有50%的正八面体空隙没有填充阳离子。图示结构中O2-离子数目为8×
=4,故正四面体空隙数与O2-离子数目之比8:4=2:1;Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,有50%的正八面体空隙没有填充阳离子。图示结构中O2-离子数目为8×![]() +6×
+6×![]() =4,则含有Fe3+和Fe2+的总数为3,晶胞中有8个图示结构单元,1mol晶胞的质量为8×(3×56+4×16)=8×232g,则晶体密度=
=4,则含有Fe3+和Fe2+的总数为3,晶胞中有8个图示结构单元,1mol晶胞的质量为8×(3×56+4×16)=8×232g,则晶体密度=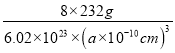 =5.18g/cm3,a=
=5.18g/cm3,a=![]() ×1010,故答案为:2∶1;50%;
×1010,故答案为:2∶1;50%; ![]() ×1010。
×1010。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案





