��Ŀ����
����Ŀ�����ܱ������н��з�ӦCH4��g��+H2O��g��![]() CO��g��+3H2��g����H��0�����c��CH4���淴Ӧʱ�䣨t���ı仯��ͼ��ʾ�������ж���ȷ���ǣ� ��
CO��g��+3H2��g����H��0�����c��CH4���淴Ӧʱ�䣨t���ı仯��ͼ��ʾ�������ж���ȷ���ǣ� ��
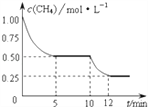
A. �����£���С���������ƽ���c��H2����С
B. 0��5min�ڣ�v��H2��=0.1mol/��Lmin��
C. 10minʱ���ı��������������������¶�
D. 12minʱ����Ӧ��ƽ��ı���ԭ�����������������ٱ仯
���𰸡�C
��������A������£���С���������ѹǿ����ƽ�������ƶ������ݻ�ѧƽ���ƶ�ԭ�����ƶ��Ľ�������ˡ�����Ũ�ȵ�������������������������Ũ�ȵ���������ƽ���c(H2)�������������A����B���ͼ��֪��0��5min�ڼ����Ũ����1.00mol/L��СΪ0.50mol/L����v(CH4)=(1.00mol/L-0.50mol/L)��5min=0.1 mol/(Lmin)����Ϊ�ò�ͬ���ʱ�ʾ�Ļ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�����v(H2)=3��0.1mol/(Lmin)=0.3 mol/(Lmin)����B����C���ͼ��֪��10minʱ�����Ũ�ȼ�����С���÷�Ӧ�����ƶ�������Ϊ�÷�Ӧ���������ȷ�Ӧ�����Կ������������¶ȣ���C��ȷ��D���ѧ��Ӧ�ﵽƽ���ʵ����������������ȣ���D������

 ��У����ϵ�д�
��У����ϵ�д�