题目内容
下列离子方程式中正确的是( )A.漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3-
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-
 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2OC.将Fe2O3溶解于足量H+溶液:Fe2O3+6H+=2Fe3++3H2O
D.KI溶液与H2SO4酸化的H2O2溶液混合:2I-+H2O2+2H+=2H2O+I2
【答案】分析:A、漂白粉溶液在空气中失效时,生成的是碳酸盐而不是碳酸氢盐,此外2HClO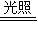 2HCl+O2↑,没有这一步关键反应就不叫漂白粉失效;
2HCl+O2↑,没有这一步关键反应就不叫漂白粉失效;
B、离子方程式的书写要遵循电荷守恒;
C、金属氧化物和强酸(非氧化性)反应生成对应的盐和水;
D、碘离子有强还原性,双氧水在酸性环境下具有氧化性,二者之间发生氧化还原反应.
解答:解:A、漂白粉溶液在空气中失效的离子方程式为:ClO-+CO2+H2O═HClO+CO32-,此外2HClO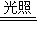 2HCl+O2↑,没有这一步关键反应就不叫漂白粉失效;故A错误;
2HCl+O2↑,没有这一步关键反应就不叫漂白粉失效;故A错误;
B、用浓盐酸与MnO2反应制取少量氯气的离子方程式为:MnO2+4H++2Cl-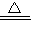 Mn2++Cl2↑+2H2O,故B错误;
Mn2++Cl2↑+2H2O,故B错误;
C、将Fe2O3溶解于足量H+溶液,氧化物溶解得到对应的盐和水,方程式为:Fe2O3+6H+=2Fe3++3H2O,故C正确;
D、碘离子有强还原性,双氧水在酸性环境下具有氧化性,反应的离子方程式为:2I-+H2O2+2H+=2H2O+I2,故D正确.
故选CD.
点评:本题主要考查学生离子方程式的正误判断方法,是现在考试的热点,难度不大.
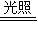 2HCl+O2↑,没有这一步关键反应就不叫漂白粉失效;
2HCl+O2↑,没有这一步关键反应就不叫漂白粉失效;B、离子方程式的书写要遵循电荷守恒;
C、金属氧化物和强酸(非氧化性)反应生成对应的盐和水;
D、碘离子有强还原性,双氧水在酸性环境下具有氧化性,二者之间发生氧化还原反应.
解答:解:A、漂白粉溶液在空气中失效的离子方程式为:ClO-+CO2+H2O═HClO+CO32-,此外2HClO
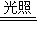 2HCl+O2↑,没有这一步关键反应就不叫漂白粉失效;故A错误;
2HCl+O2↑,没有这一步关键反应就不叫漂白粉失效;故A错误;B、用浓盐酸与MnO2反应制取少量氯气的离子方程式为:MnO2+4H++2Cl-
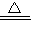 Mn2++Cl2↑+2H2O,故B错误;
Mn2++Cl2↑+2H2O,故B错误;C、将Fe2O3溶解于足量H+溶液,氧化物溶解得到对应的盐和水,方程式为:Fe2O3+6H+=2Fe3++3H2O,故C正确;
D、碘离子有强还原性,双氧水在酸性环境下具有氧化性,反应的离子方程式为:2I-+H2O2+2H+=2H2O+I2,故D正确.
故选CD.
点评:本题主要考查学生离子方程式的正误判断方法,是现在考试的热点,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目