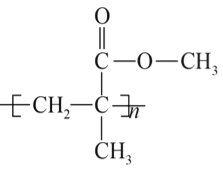
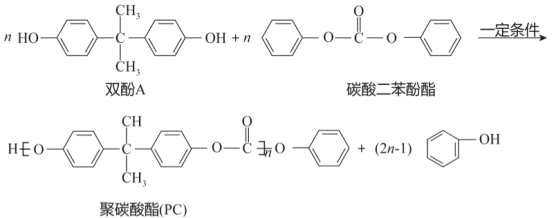
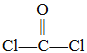��Ŀ����
����Ŀ��������M���C������أ���ͼ������ԭ���á������ܶȸߵ��ŵ㣬������Ϊ����Դ�������ƶ��豸�ĵ�Դ�������طŵ���ܷ�Ӧ����ʽΪ��4M+nO2+2nH2O=4M(OH) n����֪����ص������۱�������ָ��λ�����ĵ缫�������������ͷų��������ܡ�����˵������ȷ����

A. ���ö�缫��Ŀ������ߵ缫��������Һ�ĽӴ��������������������ɢ���缫����
B. �Ƚ�Mg��Al��Zn���ֽ����C������أ�Al�C������ص����۱��������
C. M�C������طŵ���̵�������Ӧʽ��4Mn++nO2+2nH2O+4ne�C=4M(OH)n
D. ��Mg�C��������У�Ϊ��ֹ����������Mg(OH)2���˲������Ե���ʼ������ӽ���Ĥ
���𰸡�C
��������A����Ӧ��Ӵ����Խ��Ӧ����Խ�죬���Բ��ö�缫��Ŀ������ߵ缫��������Һ�ĽӴ��������������������ɢ���缫���棬�Ӷ���߷�Ӧ���ʣ���A��ȷ��B����صġ����۱�������ָ��λ�����ĵ缫�������������ͷų��������ܣ���λ�����ĵ缫����ʧȥ���ӵ����ʵ���Խ����õ��ĵ���Խ�࣬������������1gʱ�������ֽ���ת�Ƶ������ʵ����ֱ�Ϊ![]() ��2=
��2=![]() mol��
mol��![]() ��3=
��3=![]() mol��
mol��![]() ��2=
��2=![]() mol������Al-������ص����۱�������ߣ���B��ȷ��C�������������õ��Ӻ�ˮ��Ӧ����OH-����Ϊ�������ӽ���Ĥ�����������Ӳ��ܽ�������������������ӦʽΪO2+2H2O+4e-=4OH-����C����D��������Mgʧ��������Mg2+��Ϊ��ֹ����������Mg(OH)2������������Һ���ܺ��д���OH-�������˲������Ե���ʼ������ӽ���Ĥ����D��ȷ����ѡC��
mol������Al-������ص����۱�������ߣ���B��ȷ��C�������������õ��Ӻ�ˮ��Ӧ����OH-����Ϊ�������ӽ���Ĥ�����������Ӳ��ܽ�������������������ӦʽΪO2+2H2O+4e-=4OH-����C����D��������Mgʧ��������Mg2+��Ϊ��ֹ����������Mg(OH)2������������Һ���ܺ��д���OH-�������˲������Ե���ʼ������ӽ���Ĥ����D��ȷ����ѡC��

 Сѧѧϰ�ð���ϵ�д�
Сѧѧϰ�ð���ϵ�д� Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д�����Ŀ�����û�ѧԭ���Է�������ˮ������������̼��������ʵ����ɫ�������������ã��Թ�����̬��������Ҫ���塣
��1��ȼú�����е�CO2��ת��Ϊ��������ԭ�ϡ������Դ�״���CH3OH���״��Ľṹʽ��ͼ����

3H2(g)+CO2(g) ![]() CH3OH (g) + H2O(g) ��H
CH3OH (g) + H2O(g) ��H
����֪��
��ѧ�� | C-H | C-O | C=O | H-H | O-H |
����/KJ/mol | 412 | 351 | 745 | 436 | 462 |
����H = _________________
�ڷ����е�CO2ת��Ϊ�״������������״�ȼ�ϵ�أ��ṹ��ͼ�������ӽ���Ĥ�����������Һ��Ϊ1L2mol��L-1H2SO4��Һ����ȼ�ϵ����ͨ��״���һ��Ϊ____����a��b�������������1mol e-����ת��ʱ����������Һ������֮��Ϊ______g �����跴Ӧ��ľ�������������ܽ⣩��

��2��H2��ԭ����������������
��֪�� N2(g)+2O2(g)��2NO2(g) ��H��+133kJ��mol��1
H2O(g)�� H2O(l) ��H����44kJ��mol��1
H2��ȼ����Ϊ285.8kJ��mol��1
���ڴ��������£�H2��ԭNO2����ˮ�����͵������Ȼ�ѧ����ʽΪ_____________��
�� ��H2(g)Ϊȼ�Ͽ����������ȼ�ϵ�أ��õ����ϡNaOH���������Һ���为���缫��ӦʽΪ___________________________________________________________����֪�õ�ص�����ת��Ч��Ϊ86.4%����õ�صı�����Ϊ________kW��h��kg��1(�������1λС������������![]() ��1 kW��h��3.6��106 J) ��
��1 kW��h��3.6��106 J) ��
��3������ȼ�ϵ��(MFC)��һ���ִ����İ���ȥ����������ͼΪMFC̼������ͬʱȥ����ʾ��ͼ��

����֪A��B��������CO2��N2�����ʵ���֮��Ϊ5 : 2��д��A���ĵ缫��Ӧʽ____________________________________________��
�ڽ���װ��ȥ��NH4+��ԭ��_______________________________________________��
��4�������� Na��CO2����ؿɽ�CO2���Ϊ����

�ҹ�������Ա���Ƴ��Ŀɳ���� Na��CO2����أ����Ʋ��Ͷ��̼���ܣ�MWCNT��Ϊ�缫���ϣ���Ӧǰ���缫������ȣ����ܷ�ӦΪ4Na+3CO2![]() 2Na2CO3+C���ŵ�ʱ�õ����������CO2���乤��ԭ����ͼ��ʾ��
2Na2CO3+C���ŵ�ʱ�õ����������CO2���乤��ԭ����ͼ��ʾ��
�ٷŵ�ʱ�������ĵ缫��ӦʽΪ______________________��
�������ɵ�Na2CO3��Cȫ�������ڵ缫���棬��ת��0.2 mol e-ʱ��������������Ϊ_________g��
����Ŀ����֪25�桢101kPaʱ��һЩ���ʵ�ȼ����Ϊ���ش��������⣺
��ѧʽ | CO(g) | H2(g) | CH3OH(l) | CH4(g) |
��H/(kJ��mol-l) | -283.0 | -285.8 | -726.5 | -890.3 |
��1��д����������CH3OH(l)��ȫȼ�յ��Ȼ�ѧ����ʽ��_____________________________��
��2�����ݸ�˹����������з�Ӧ���Ȼ�ѧ����ʽ��CO(g)+2H2(g)![]() CH3OH(l)��H=__________��
CH3OH(l)��H=__________��
��3����ҵ������ˮú���ϳɼ״�����Ҫ��Ӧ�ɱ�ʾΪ![]() CO(g)+H2(g)
CO(g)+H2(g)![]()
![]() CH3OH(g)��H=-45.4kJ��mol-1�����ݻ�Ϊ1L���ܱ������м���0.10molH2��0.05molCO����һ���¶��·���������Ӧ��10min��Ӧ�ﵽƽ��״̬����÷ų�����3.632kJ��
CH3OH(g)��H=-45.4kJ��mol-1�����ݻ�Ϊ1L���ܱ������м���0.10molH2��0.05molCO����һ���¶��·���������Ӧ��10min��Ӧ�ﵽƽ��״̬����÷ų�����3.632kJ��
����ͬ�¶������£�������Ӧ�Ļ�ѧƽ�ⳣ��K=___________��
���������ݻ����䣬���д�ʩ������CH3OH���ʵ���___________ (����)��
a�������¶�
b����CH3OH(g)����ϵ�з���
c������He��ʹ��ϵ��ѹǿ����
d���ٳ���0.10molH2��0.05molCO
e���������
�۷�Ӧ�ﵽƽ����������������䣬��ֻ�������������Сһ�룬ƽ�⽫___________(�����������)�ƶ�����ѧƽ�ⳣ��K___________(�������С�����䡱)��
���¶ȡ��ݻ���ͬ�ļס��������ܱ������������м���1molCO��2molH2�����м���lmolCH3OH(g)����Ӧ�ﵽƽ��ʱ�ų�������ΪQ1kJ�������յ�����ΪQ2kJ������CO��ת����Ϊa1������CH3OH��ת����Ϊa2����Q1+Q2=___________��a1+a2=___________��