题目内容
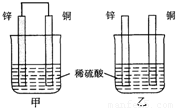
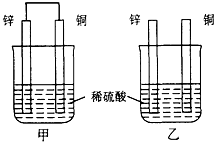 将纯锌片和纯铜片按如图方式插入100ml相同浓度的稀硫酸中一段时间,请回答下列问题:
将纯锌片和纯铜片按如图方式插入100ml相同浓度的稀硫酸中一段时间,请回答下列问题:(1)下列说法正确的是
BD
BD
.A、甲、乙均为化学能转变为电能的装置
B、乙中铜片上没有明显变化
C、甲中铜片质量减少、乙中锌片质量减少
D、两烧杯中溶液的pH均增大
(2)在相同时间内,两烧杯中产生气泡的速度:甲
>
>
乙(填“>”、“<“或“=”).(3)当甲中产生1.12L(标准状况)气体时,通过导线的电子为
0.1
0.1
mol.(4)这时,甲中负极发生氧化反应,溶解了
3.25
3.25
g.分析:(1)甲装置符合原电池构成条件,所以是原电池,乙不能形成闭合回路,所以不能构成原电池,两个烧杯中,锌都失电子发生氧化反应,甲中铜上氢离子得电子发生还原反应,乙中锌上氢离子得电子发生还原反应;
(2)作原电池负极的金属加速被腐蚀;
(3)根据氢气和转移电子之间的关系式计算;
(4)根据甲中氢气和锌之间的关系式计算.
(2)作原电池负极的金属加速被腐蚀;
(3)根据氢气和转移电子之间的关系式计算;
(4)根据甲中氢气和锌之间的关系式计算.
解答:解:(1)A、甲符合原电池构成条件,所以属于原电池,乙不能构成闭合回路,所以不能构成原电池,故A错误;
B、乙不能构成原电池,氢离子在锌片上得电子发生还原反应,所以乙中铜片上没有明显变化,故B正确;
C、甲中铜片作正极,正极上氢离子得电子生成氢气,所以铜片质量不变,乙中锌片和氢离子发生置换反应,所以质量减少,故C错误;
D、两烧杯中锌和氢离子发生置换反应导致溶液中氢离子浓度减小,所以溶液的pH均增大,故D正确;
故选:BD;
(2)甲能构成原电池,乙不能构成原电池,作原电池负极的金属加速被腐蚀,所以在相同时间内,两烧杯中产生气泡的速度:甲>乙,故答案为:>;
(3)甲中,铜电极上氢离子得电子生成氢气,电极反应式为2H++2e-=H2↑,根据电极反应式知,通过电子的物质的量=
×2=0.1mol,
故答案为:0.1;
(4)甲中负极锌上电极反应式为Zn-2e-=Zn2+,正极电极反应式为2H++2e-=H2↑,根据锌和氢气之间的关系式知,溶解锌的质量=
×65g/mol=3.25g,
故答案为:3.25.
B、乙不能构成原电池,氢离子在锌片上得电子发生还原反应,所以乙中铜片上没有明显变化,故B正确;
C、甲中铜片作正极,正极上氢离子得电子生成氢气,所以铜片质量不变,乙中锌片和氢离子发生置换反应,所以质量减少,故C错误;
D、两烧杯中锌和氢离子发生置换反应导致溶液中氢离子浓度减小,所以溶液的pH均增大,故D正确;
故选:BD;
(2)甲能构成原电池,乙不能构成原电池,作原电池负极的金属加速被腐蚀,所以在相同时间内,两烧杯中产生气泡的速度:甲>乙,故答案为:>;
(3)甲中,铜电极上氢离子得电子生成氢气,电极反应式为2H++2e-=H2↑,根据电极反应式知,通过电子的物质的量=
| 1.12L |
| 22.4L/mol |
故答案为:0.1;
(4)甲中负极锌上电极反应式为Zn-2e-=Zn2+,正极电极反应式为2H++2e-=H2↑,根据锌和氢气之间的关系式知,溶解锌的质量=
| ||
| 2 |
故答案为:3.25.
点评:本题考查了原电池原理,明确正负极上发生的电极反应是解本题关键,根据电极反应式来分析解答即可,难度不大.

练习册系列答案
相关题目
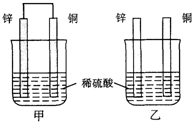 将纯锌片和纯铜片按如图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
将纯锌片和纯铜片按如图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )| A、甲中铜片是负极 | B、两烧杯中铜片表面均无气泡产生 | C、产生气泡的速度甲比乙快 | D、两烧杯中溶液的pH均减小 |
 (2008?乐山一模)将纯锌片和纯铜片按如图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
(2008?乐山一模)将纯锌片和纯铜片按如图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )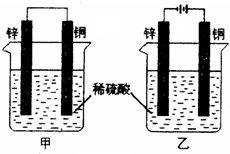 将纯锌片和纯铜片按如图所示方式插入同浓度的稀H2SO4中一段时间,以下叙述正确的是( )
将纯锌片和纯铜片按如图所示方式插入同浓度的稀H2SO4中一段时间,以下叙述正确的是( )