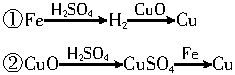题目内容
用一定量的铁与足量的CuO制单质铜,有人设计了以下两种方案:
①Fe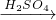 H2
H2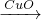 Cu ②CuO
Cu ②CuO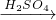 CuSO4
CuSO4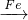 Cu
Cu
若按实验原则进行操作,则两者制得单质铜的量
- A.一样多
- B.①多
- C.②多
- D.无法判断
C
分析:写出两个方案中所发生的反应的化学方程式,根据质量守恒定律及氢气还原氧化铜的实验步骤进行分析解答.
解答:两方案中所发生的化学方程式为:①Fe+H2SO4═FeSO4+H2↑;H2+CuO Cu+H2O;
Cu+H2O;
②CuO+H2SO4═CuSO4+H2O;Fe+CuSO4═Cu+FeSO4;
方案①中氢气还原氧化铜实验,开始时需先通入一部分氢气,排除装置中的空气,实验结束时还要通一会氢气,以防止生成的铜被氧化,如果不考虑先通后停,相同质量的铁生成铜的质量是相同的,但是由于部分氢气被浪费,从而导致铁的质量被多消耗一部分,所以导致方案①对应的铜减少.故方案②生成的铜多,分析选项可知选项C是正确的;
故选 C.
点评:本题考查了制备物质的不同途径中,方案不同,产物不同;生成产物的量的多少由反应物决定,参加反应的物质要根据实验过程实际用量进行确定.
分析:写出两个方案中所发生的反应的化学方程式,根据质量守恒定律及氢气还原氧化铜的实验步骤进行分析解答.
解答:两方案中所发生的化学方程式为:①Fe+H2SO4═FeSO4+H2↑;H2+CuO
 Cu+H2O;
Cu+H2O;②CuO+H2SO4═CuSO4+H2O;Fe+CuSO4═Cu+FeSO4;
方案①中氢气还原氧化铜实验,开始时需先通入一部分氢气,排除装置中的空气,实验结束时还要通一会氢气,以防止生成的铜被氧化,如果不考虑先通后停,相同质量的铁生成铜的质量是相同的,但是由于部分氢气被浪费,从而导致铁的质量被多消耗一部分,所以导致方案①对应的铜减少.故方案②生成的铜多,分析选项可知选项C是正确的;
故选 C.
点评:本题考查了制备物质的不同途径中,方案不同,产物不同;生成产物的量的多少由反应物决定,参加反应的物质要根据实验过程实际用量进行确定.

练习册系列答案
相关题目
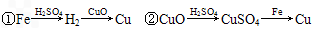 若按实验原则进行操作,则两者制得单质铜的量的比较中,正确的是
若按实验原则进行操作,则两者制得单质铜的量的比较中,正确的是