题目内容
【题目】下列叙述中正确的是
A. 直径介于l~100 nm之间的粒子被称为胶体
B. 电泳现象可证明胶体带电荷
C. 利用丁达尔现象可区别溶液和胶体
D. 胶体粒子很小,但不能通过滤纸
【答案】C
【解析】A. 微粒直径介于l~100 nm之间的分散系称为胶体,A错误;B. 电泳现象可证明胶体的胶粒带电荷,胶体不带电荷,B错误;C. 胶体可以产生丁达尔效应,利用丁达尔现象可区别溶液和胶体,C正确;D. 胶体粒子很小,但能通过滤纸,不能透过半透膜,D错误,答案选C。

【题目】决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
A | 578 | 1817 | 2745 | 11578 |
B | 738 | 1451 | 7733 | 10540 |
A通常显价,B元素的核外电子排布式为。
(2)波长为300nm紫外光的光子所具有的能量约为399 kJ·mol-1。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因是。组成蛋白质的最简单的氨基酸中的碳原子杂化类型是。
共价键 | C-C | C-N | C-S |
键能/ kJ·mol-1 | 347 | 305 | 259 |
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构
与NaCl晶体结构相似(如下图所示),已知3种离子晶体的晶格能数据如下表: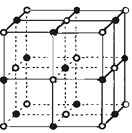
离子晶体 | NaCl | KCl | CaO |
晶格能/kJ·mol-1 | 786 | 715 | 3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是。其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有个。
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是。
(5)某配合物的分子结构如下图所示,其分子内不含有(填序号)。
A.离子键
B.极性键
C.金属键
D.配位键
E.氢键
F.非极性键
