题目内容
实验测得常温下0.1 mol·L-1某一元酸(HA)溶液的pH不为1,0.1 mol·L-1某一元碱(BOH)溶液中A.c(A-)>c(B+)>c(H+)>c(OH-) B.c(B+)>c(A-)>c(OH-)>c(H+)
C.c(B+)=c(A-)>c(OH-)=c(H+) D.c(B+)>c(A-)>c(H+)>c(OH-)
解析:0.1 mol·L-1的HA酸pH不为1,说明该酸为弱酸。0.1 mol·L-1的BOH溶液在常温下,c(H+)·c(OH-)=10-14,又由题可知,c(H+)/c(OH-)=10-12即c(H+)=10-12·c(OH-),所以[c(OH)-]2=10-2,c(OH-)=10-11 mol·L-1,即c(OH-)=c(BOH)=0.1 mol·L-1,所以BOH是一元强碱,此两种溶液等体积混合,恰好完全反应,生成BA强碱弱酸盐,A-部分水解,溶液呈碱性。溶液中各离子浓度排序为c(B+)>c(A-)>c(OH-)>c(H+),B项正确。
答案:B

练习册系列答案
相关题目
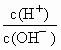 =10-12,将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度由大到小顺序是
=10-12,将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度由大到小顺序是