��Ŀ����
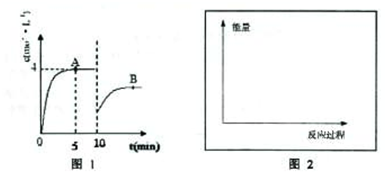
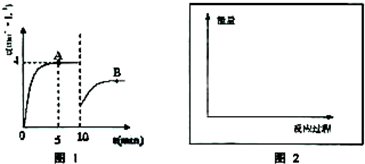
��һ�������£��ϳ����е�������������ʼŨ�ȷֱ�Ϊa mol?L-1��b mol?L-1����ӦΪ��N2+3H2��2NH3��������Ũ����ʱ��仯��ͼ1��ʾ��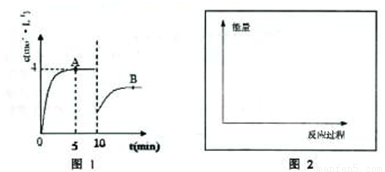
��1����Ӧ��5minʱ��������Ӧ����______��
��2����10minʱ��ȡ�Ĵ�ʩ��______��A��ƽ�ⳣ��Ϊ______����A��ƽ�ⳣ��K______�����������������=����B���ƽ�ⳣ����
��3�����ϳ���������17g�����ų�45.5kJ��������ͼ2�����ϻ����úϳɰ���Ӧ������������ʱ��ı仯ʾ��ͼ��
��4��-50°Cʱ��Һ���������µ��룺2NH3?NH4++NH-2��k=2×10-2��Һ���ĵ���ﵽƽ��ʱ��������Ũ�ȴ�С��ϵΪ______������NH4Cl���壬K______2×10-12�����������������=����
���𰸡���������1���ɷ�Ӧ����Ϊ��λʱ����Ũ�ȵı仯�������㰱���ķ�Ӧ���ʣ������÷�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȼ��������ķ�Ӧ���ʣ�
��2����ͼ��֪10minʱ������Ũ��˲���С��ƽ�ⳣ��Ϊ������Ũ����֮���뷴Ӧ��Ũ����֮�ȵıȣ��¶Ȳ��䣬��ѧƽ��K���䣻
��3������17g�����ų�46.6kJ������������1molNH3�ų�����46.6kJ����Ӧ��������ߣ�������������ͣ�
��4������ij̶Ȳ����ɵ��뷽��ʽ��֪��c��NH+4��=c��NH-2�����¶Ȳ��䣬����ƽ�ⳣ�����䣮
����⣺��1��5minʱ������Ũ��Ϊ4mol/L�������ķ�Ӧ����Ϊ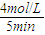 =0.8mol?L-1?min-1��
=0.8mol?L-1?min-1��
�ɷ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȿ�֪�������ķ�Ӧ����Ϊ0.8mol?L-1?min-1× =1.2mol?L-1?min-1��
=1.2mol?L-1?min-1��
�ʴ�Ϊ��1.2mol?L-1?min-1��
��2����ͼ��֪10minʱ������Ũ��˲���С�����ȡ�Ĵ�ʩΪ��ȥ���ְ�����
��N2+3H2��2NH3��
��ʼa b 0
ת��2 6 4
ƽ��a-2 b-6 4
��K= ��
��
��A��B����¶���ԣ���ѧƽ�ⳣ��K��ȣ��ʴ�Ϊ����ȥ���ְ�����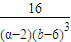 ��=��
��=��
��3���������֪����1molNH3�ų�����46.6kJ����Ӧ��������ߣ�������������ͣ���ͼ ��
��
�ʴ�Ϊ�� ��
��
��4�������ij̶Ȳ����ɵ��뷽��ʽ��֪��c��NH+4��=c��NH-2������c��NH3����c��NH+4��=c��NH-2�������¶Ȳ��䣬����ƽ�ⳣ��K���䣬
�ʴ�Ϊ��c��NH3����c��NH+4��=c��NH-2����=��
���������⿼�黯ѧ��Ӧ���ʡ���ѧƽ���ƶ���ƽ�ⳣ���������֪ʶ����ȷͼ��ͼ��ķ����ǽ����Ĺؼ����ѶȽϴ�
��2����ͼ��֪10minʱ������Ũ��˲���С��ƽ�ⳣ��Ϊ������Ũ����֮���뷴Ӧ��Ũ����֮�ȵıȣ��¶Ȳ��䣬��ѧƽ��K���䣻
��3������17g�����ų�46.6kJ������������1molNH3�ų�����46.6kJ����Ӧ��������ߣ�������������ͣ�
��4������ij̶Ȳ����ɵ��뷽��ʽ��֪��c��NH+4��=c��NH-2�����¶Ȳ��䣬����ƽ�ⳣ�����䣮
����⣺��1��5minʱ������Ũ��Ϊ4mol/L�������ķ�Ӧ����Ϊ
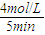 =0.8mol?L-1?min-1��
=0.8mol?L-1?min-1���ɷ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȿ�֪�������ķ�Ӧ����Ϊ0.8mol?L-1?min-1×
 =1.2mol?L-1?min-1��
=1.2mol?L-1?min-1���ʴ�Ϊ��1.2mol?L-1?min-1��
��2����ͼ��֪10minʱ������Ũ��˲���С�����ȡ�Ĵ�ʩΪ��ȥ���ְ�����
��N2+3H2��2NH3��
��ʼa b 0
ת��2 6 4
ƽ��a-2 b-6 4
��K=
 ��
����A��B����¶���ԣ���ѧƽ�ⳣ��K��ȣ��ʴ�Ϊ����ȥ���ְ�����
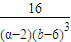 ��=��
��=����3���������֪����1molNH3�ų�����46.6kJ����Ӧ��������ߣ�������������ͣ���ͼ
 ��
���ʴ�Ϊ��
 ��
����4�������ij̶Ȳ����ɵ��뷽��ʽ��֪��c��NH+4��=c��NH-2������c��NH3����c��NH+4��=c��NH-2�������¶Ȳ��䣬����ƽ�ⳣ��K���䣬
�ʴ�Ϊ��c��NH3����c��NH+4��=c��NH-2����=��
���������⿼�黯ѧ��Ӧ���ʡ���ѧƽ���ƶ���ƽ�ⳣ���������֪ʶ����ȷͼ��ͼ��ķ����ǽ����Ĺؼ����ѶȽϴ�

��ϰ��ϵ�д�
�����Ŀ