题目内容
以NA表示阿伏伽德罗常数的值,下列说法中正确的是几种
①58.5g氯化钠固体中含有NA个氯化钠分子;
②5.6g铁粉与酸反应失去的电子数一定为0.3NA;
③4.5g SiO2晶体中含有的共价键数为0.3NA;
④标况下,11.2L SO3所含的分子数为0.5NA;
⑤1mol FeCl3完全水解转化为氢氧化铁胶体后生成NA个胶粒;
⑥常温下,42g C2H4和C4H8的混合物中含有的碳原子数为3NA
⑦10g质量分数为46%的乙醇溶液中,氢原子的总数为1.2NA
⑧1mol C10H22分子中含有的共价键数目为32NA
⑨在含有NA个醋酸根离子(CH3COO-)的醋酸溶液中氢离子数目为NA
⑩标准状况下,22.4LCH4和CH3OH的混合物中含有NA个碳原子.
- A.1种
- B.3种
- C.4种
- D.5种
A
分析:①氯化钠固体中不存在氯化钠分子;
②铁粉与酸反应生成亚铁离子也可以生成铁离子;
③质量换算物质的量结合1mol二氧化硅中含4mol硅氧键;
④标况下,SO3不是气体;
⑤氢氧化铁胶体胶粒是氢氧化铁的集合体;
⑥C2H4和C4H8的最简式相同,只需计算42gCH2中含有的碳原子数;
⑦10g质量分数为46%的乙醇溶液中计算乙醇物质的量,结合分子式计算氢原子的总数;
⑧1mol C10H22分子中结合烷烃分子结构计算含有的共价键数目;
⑨在含有NA个醋酸根离子(CH3COO-)的醋酸溶液中存在水的电离;
⑩标准状况下,22.4LCH4和CH3OH的混合物中含有NA个碳原子.甲醇在标准状况下不是气体.
解答:①58.5g氯化钠固体物质的量为1mol,氯化钠是由离子构成的,不存在分子;故①错误;
②5.6g铁粉物质的量为0.1mol,与强氧化性酸反应失去的电子数为0.3NA;与稀酸反应生成二价铁盐,失去电子为0.2mol,故②错误;
③4.5g SiO2晶体物质的量为0.09mol,1mol 二氧化硅中含4mol 共价键,所以0.09mol 晶体中中含有的共价键数为0.36NA;故③错误;
④标况下,11.2L SO3所含的分子数为0.5NA;三氧化硫在标准状况下不是气体,11.2L SO3所物质的量不是0.5mol,故④错误;
⑤1mol FeCl3完全水解转化为氢氧化铁胶体,氢氧化铁假体微粒是氢氧化铁的集合体,生成胶粒小于NA个;故⑤错误;
⑥常温下,42g C2H4和C4H8的混合物中含有的碳原子数,只需计算42gCH2中碳原子数=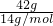 =3NA,故⑥正确;
=3NA,故⑥正确;
⑦10g质量分数为46%的乙醇溶液中溶质乙醇的物质的量=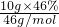 =0.1mol,氢原子的总数为0.6NA,故⑦错误;
=0.1mol,氢原子的总数为0.6NA,故⑦错误;
⑧1mol C10H22分子中含有的共价键数目=1mol×(10-1+22)×NA=31NA,故⑧错误;
⑨在含有NA个醋酸根离子(CH3COO-)的醋酸溶液中,存在水的电离,氢离子数目大于NA,故⑨错误;
⑩标准状况下,22.4L CH4和CH3OH的混合物中含有NA个碳原子.甲醇在标准状况下是液体,故⑩错误;
综上所述:有一种正确;
故选A.
点评:本题考查了阿伏伽德罗常的应用,主要考查质量换算物质的量计算微粒数,晶体结构,胶体的组成,分子中的化学键计算,弱电解质溶液中两种判断,气体摩尔体积的体积应用,综合性较强.
分析:①氯化钠固体中不存在氯化钠分子;
②铁粉与酸反应生成亚铁离子也可以生成铁离子;
③质量换算物质的量结合1mol二氧化硅中含4mol硅氧键;
④标况下,SO3不是气体;
⑤氢氧化铁胶体胶粒是氢氧化铁的集合体;
⑥C2H4和C4H8的最简式相同,只需计算42gCH2中含有的碳原子数;
⑦10g质量分数为46%的乙醇溶液中计算乙醇物质的量,结合分子式计算氢原子的总数;
⑧1mol C10H22分子中结合烷烃分子结构计算含有的共价键数目;
⑨在含有NA个醋酸根离子(CH3COO-)的醋酸溶液中存在水的电离;
⑩标准状况下,22.4LCH4和CH3OH的混合物中含有NA个碳原子.甲醇在标准状况下不是气体.
解答:①58.5g氯化钠固体物质的量为1mol,氯化钠是由离子构成的,不存在分子;故①错误;
②5.6g铁粉物质的量为0.1mol,与强氧化性酸反应失去的电子数为0.3NA;与稀酸反应生成二价铁盐,失去电子为0.2mol,故②错误;
③4.5g SiO2晶体物质的量为0.09mol,1mol 二氧化硅中含4mol 共价键,所以0.09mol 晶体中中含有的共价键数为0.36NA;故③错误;
④标况下,11.2L SO3所含的分子数为0.5NA;三氧化硫在标准状况下不是气体,11.2L SO3所物质的量不是0.5mol,故④错误;
⑤1mol FeCl3完全水解转化为氢氧化铁胶体,氢氧化铁假体微粒是氢氧化铁的集合体,生成胶粒小于NA个;故⑤错误;
⑥常温下,42g C2H4和C4H8的混合物中含有的碳原子数,只需计算42gCH2中碳原子数=
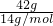 =3NA,故⑥正确;
=3NA,故⑥正确;⑦10g质量分数为46%的乙醇溶液中溶质乙醇的物质的量=
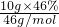 =0.1mol,氢原子的总数为0.6NA,故⑦错误;
=0.1mol,氢原子的总数为0.6NA,故⑦错误;⑧1mol C10H22分子中含有的共价键数目=1mol×(10-1+22)×NA=31NA,故⑧错误;
⑨在含有NA个醋酸根离子(CH3COO-)的醋酸溶液中,存在水的电离,氢离子数目大于NA,故⑨错误;
⑩标准状况下,22.4L CH4和CH3OH的混合物中含有NA个碳原子.甲醇在标准状况下是液体,故⑩错误;
综上所述:有一种正确;
故选A.
点评:本题考查了阿伏伽德罗常的应用,主要考查质量换算物质的量计算微粒数,晶体结构,胶体的组成,分子中的化学键计算,弱电解质溶液中两种判断,气体摩尔体积的体积应用,综合性较强.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目