题目内容
【题目】10mL浓度为1molL-1的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应率但又不影响氢气生成量的是( )
A.H2SO4B.K2SO4C.Na2CO3D.CuSO4
【答案】B
【解析】
A.加入H2SO4溶液,导致溶液中氢离子浓度增大或减小,反应速率不能确定,与题意不符,A错误;
B.加入K2SO4溶液,对原溶液有稀释作用,且不反应,导致溶液中氢离子浓度减小,反应速率减慢,符合题意,B正确;
C.加入Na2CO3溶液,消耗氢离子生成二氧化碳,导致生成氢气的量减少,与题意不符,C错误;
D.加入CuSO4溶液,锌置换出铜,形成锌铜原电池,锌作负极,导致生成氢气的速率加快,与题意不符,D错误;
答案为B。

练习册系列答案
相关题目
【题目】已知: ①1mol晶体硅中含有2molSi-Si键。②Si(s)+O2(g)=SiO2(s)ΔH,其反应过程与能量变化如图所示。
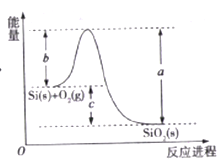
③
化学键 | Si-O | O=O | Si-Si |
断开1mol共价键所需能量/KJ | 460 | 500 | 176 |
下列说法正确的是
A. 晶体硅光伏发电是将化学能转化为电能的
B. 二氧化硅稳定性小于硅的稳定性
C. ΔH=-988 kJ/mol
D. ΔH=a-c